Nat Cancer:南方医科大学汪枭睿团队报告了一种同时抑制肿瘤生长和转移的治疗新范式!
2025-06-27 iNature iNature 发表于上海
该研究表明脂质化纳米光敏剂追踪和禁用肿瘤细胞外囊泡同时抑制肿瘤生长和转移。
癌症细胞通过肿瘤细胞外囊泡(TEV)介导的细胞间和组织间通讯促进肿瘤生长和转移。抑制TEV是一种有前景的抑制转移的策略;有效和选择性地禁用TEV仍然具有挑战性。
2025年6月24日,南方医科大学汪枭睿团队在Nature Cancer在线发表题为“Concurrent inhibition of tumor growth and metastasis by a lipidated nanophotosensitizer tracing and disabling tumor extracellular vesicles”的研究论文,该研究表明脂质化纳米光敏剂追踪和禁用肿瘤细胞外囊泡同时抑制肿瘤生长和转移。
该研究使用相邻的亲水性分子工程策略开发了棕榈酸表面显示的纳米粒子。出乎意料的是,这些脂质化纳米颗粒不仅被有效地吸收并分布在肿瘤细胞内,而且与TEV的产生相结合,从而能够主动追踪TEV。利用其双重肿瘤空间分布(细胞内和TEV内),构建了一种脂质化纳米光敏剂用于转移治疗。在原发肿瘤部位的近红外光照射下,细胞内和TEV内的活性氧物种同步产生。这导致了原发性肿瘤的光动力抑制,并通过禁用TEV阻断了细胞间和组织间的通讯,有效地抑制了雌性小鼠多种肿瘤模型中的肿瘤生长和转移。总体而言,这项工作报告了一种同时抑制肿瘤生长和转移的治疗范式。

肿瘤转移和复发仍然是有效治疗癌症的主要障碍。转移级联涉及肿瘤细胞通过血液或淋巴系统向远处器官的多步扩散,使手术或放疗等局部治疗不足以根除疾病。目前的治疗方案通常将手术、化疗、放疗或光动力疗法(PDT)与免疫疗法相结合,以抑制肿瘤生长和转移。然而,治疗诱导的应激可以刺激肿瘤细胞外囊泡(TEV)和可溶性因子的释放,促进转移并将肿瘤微环境重塑为免疫抑制,最终影响疗效。此外,这些方法通常与持续时间长、成本高和免疫相关毒性有关。这些局限性强调了需要更安全、更有效的抗转移策略。
转移与远处器官中允许的转移前生态位的形成密切相关。TEV已成为这一过程中细胞间和组织间通讯的关键介质。这些膜包膜异质囊泡可分为大微泡(200-2,000 nm) 和小外泌体(40-200 nm)。它们携带功能性货物,如核酸和蛋白质,调节多种促转移途径,包括血管生成、细胞外基质重塑、免疫抑制和耐药性。TEV诱导的转移前小生境促进癌症的进展。最近的研究表明,富含程序性细胞死亡蛋白1配体1(PDL1)的TEV通过损害T细胞功能和抵抗免疫检查点阻断(ICB)治疗来促进免疫逃避。乳腺癌症细胞来源的外泌体通过Lin28B调节中性粒细胞表型和T细胞免疫状态,形成免疫抑制性肺转移前生态位,以支持癌症进展。肿瘤源性外泌体肿瘤生长因子-β1(TGFβ1)通过重塑肺血管niche33促进肺微转移中的三阴性乳腺癌症细胞扩散。因此,阻断TEV-介导的通信可能为癌症患者提供一种有前景的治疗策略。
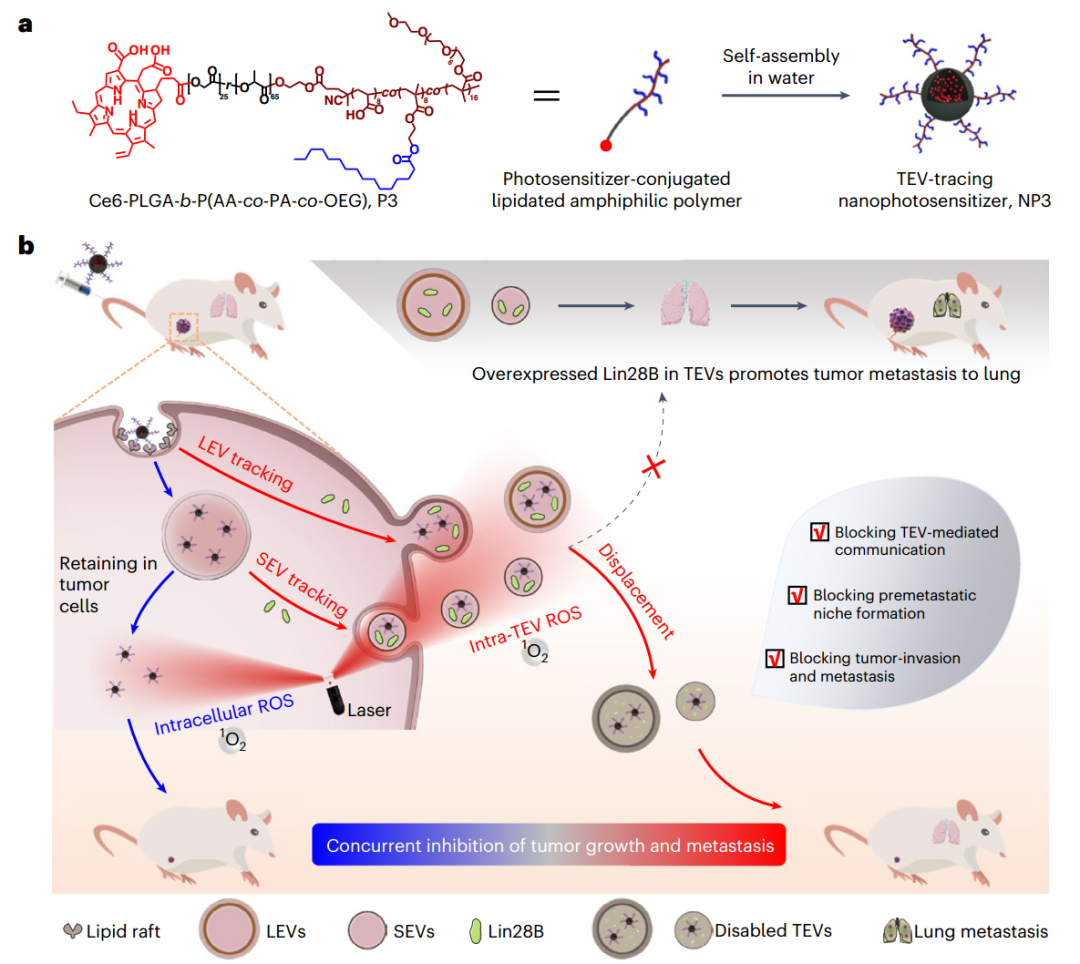
NP3追踪和禁用TEV同时抑制肿瘤生长和转移的治疗机制(图源自Nature Cancer)
已经提出了多种策略来抑制TEV功能,包括阻断囊泡生物合成、物理清除和功能性货物的中和。具体而言,药物制剂,如Nexinhibi20、替吡法尼、GW4869和麦努霉素A,用于抑制外泌体的生物发生和分泌,以减缓癌症的进展。然而,应该指出的是,EVs几乎是由所有类型的细胞产生的,具有多种基本的生物功能,包括细胞外通讯、物质分泌和废物清除。目前的外泌体抑制剂靶向正常细胞和肿瘤细胞之间共享的生化过程,导致选择性差。或者,对小TEV具有高结合能力的功能化阳离子纳米片已被证明可以清除小TEV并抑制放射治疗后的肿瘤转移。
在这里,研究人员使用相邻的亲水性分子工程策略开发了一种表面显示棕榈酸(PA)的脂质化纳米粒子平台。这些脂质化纳米粒子表现出肿瘤特异性摄取和TEV的活性追踪。这种独特的特性被定义为双肿瘤空间分布,指的是同时进行细胞内和TEV内定位。利用这一特性,构建了一种用于肿瘤转移治疗的TEV追踪纳米光敏剂。在原发肿瘤部位的近红外光照射下,细胞内和TEV内的活性氧(ROS)同步产生。该策略不仅抑制了原发性肿瘤的生长,还破坏了TEV介导的细胞间通讯,从而有效抑制了转移。值得注意的是,与抗PDL1治疗相结合,该系统被发现可以大大增强免疫协同治疗的效果。
参考信息:
https://www.nature.com/articles/s43018-025-00997-0#Sec50
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#肿瘤细胞外囊泡# #TEV#
3 举报