Nat Med:北京大学鲁智豪研究发现BL-B01D1治疗转移性食管鳞癌疗效显著且安全可控
10小时前 iNature iNature 发表于上海
该研究展示了 BL-B01D1 在 82 例既往接受过 ESCC 治疗的患者中进行的 I 期临床研究的安全性和有效性数据。
对于免疫治疗后病情进展的晚期食管鳞状细胞癌 (ESCC) 患者的研究仍然有限。BL-B01D1 是一类首创的抗体-药物偶联物,由 EGFR-HER3 双特异性抗体通过可裂解的连接体与拓扑异构酶 I 抑制剂 (Ed-04) 有效载荷结合而成。
2025年7月10日,北京大学鲁智豪独立通讯在Nature Medicine 在线发表题为“A bispecific antibody–drug conjugate targeting EGFR and HER3 in metastatic esophageal squamous cell carcinoma: a phase 1b trial”的研究论文。该研究展示了 BL-B01D1 在 82 例既往接受过 ESCC 治疗的患者中进行的 I 期临床研究的安全性和有效性数据。
主要终点是推荐的 II 期剂量。给药剂量为每 3 周 (Q3W) 输注 2.0 (n = 22) 和 2.5 (n = 60) mg kg−1 D1D8。所有患者的确认客观缓解率 (cORR) 为 29.3% (82 例中的 24 例),可评估患者的确认客观缓解率 (cORR) 为 32.9% (73 例中的 24 例)。对于接受 2.5 mg kg-1 剂量治疗的患者,cORR 为 39.6% (21/53),疾病控制率为 79.2% (42/53)。在 2.0 mg kg-1 组中,cORR 为 15.0% (3/20),疾病控制率为 50.0% (10/20)。II 期剂量确定为 2.5 mg kg-1 D1D8 Q3W。2.5 mg kg-1 剂量组 G3 治疗相关不良事件的发生率为 63.3%;最常见的不良事件是贫血(28.3%)、白细胞减少和血小板减少(各 18.3%)以及中性粒细胞减少(16.7%)。观察到两例 ≥G3 间质性肺病。总体而言,BL-B01D1 在转移性食管鳞状细胞癌患者中表现出良好的疗效和可控的安全性。进一步的 3 期临床试验已启动。ClinicalTrials.gov 注册号:NCT05262491。

食管癌是第十一大常见恶性肿瘤,也是癌症相关死亡的第七大原因。食管鳞状细胞癌 (ESCC) 是世界上最常见的食管癌类型。免疫检查点抑制剂 (ICI),例如抗程序性细胞死亡蛋白 1 (PD-1)、程序性细胞死亡配体 1 (PD-L1) 和细胞毒性 T 淋巴细胞相关抗原 4 (CTLA-4),与铂类化疗相结合,已经成为晚期 ESCC 的标准治疗方法,并具有显著的生存益处。然而,只有 10-20% 的 ESCC 患者能够长期生存,因为大多数患者对这些药物产生了耐药性。晚期 ESCC 的二线治疗包括使用伊立替康,其疗效也有限。伊立替康的客观反应率 (ORR) 不超过 10%。因此,迫切需要开发新的有效的治疗策略来克服当前疗法的局限性并提高 ESCC 患者的生存率。
表皮生长因子受体 (EGFR) 是一种受体酪氨酸激酶。它属于 v-erb-b2 成红细胞白血病病毒癌基因 (ErbB)/人类表皮受体 (HER) 家族,该家族包含四种蛋白:EGFR/HER1、ERBB2/HER2、ERBB3/HER3 和 ERBB4/HER4。50%-70% 的食管鳞状细胞癌 (ESCC) 患者存在 EGFR 过表达,且该过表达与肿瘤侵袭性和不良生存结局相关。尽管食管鳞状细胞癌 (ESCC) 患者普遍存在 EGFR 过表达,但目前的抗 EGFR 疗法(例如西妥昔单抗、帕尼单抗和吉非替尼)在改善总生存期 (OS) 方面显示出有限的益处。最近的研究表明,EGFR 和 HER3 常在各种胃肠道癌症中共表达,并与肿瘤的发生发展相关。 HER3是ErbB家族中一个独特的假激酶受体,已知其可介导抗EGFR疗法的耐药性。此外,临床前研究发现,同时靶向EGFR和HER3能够使EGFR-EGFR同型二聚体和EGFR-HER3异型二聚体结合,从而阻断其下游信号通路。因此,同时靶向EGFR和HER3有望为胃肠道癌症患者提供广谱、全肿瘤杀伤疗法。尽管已报道了若干靶向EGFR和/或HER3的药物,包括双特异性抗体和抗体-药物偶联物(ADCs),其中一些已在1期和2期研究中显示出初步疗效,但目前尚无任何药物在食管鳞状细胞癌(ESCC)患者群体中取得成功。
BL-B01D1是一款潜在的首创ADC,由EGFR×HER3双特异性抗体通过可裂解的连接体与拓扑异构酶I抑制剂(Ed-04)有效载荷结合而成。 BL-B01D1 特异性结合肿瘤细胞表面的 EGFR 和/或 HER3,通过内吞作用进入细胞,并在酶促裂解后释放 Ed-04 进入溶酶体。这反过来会阻断 DNA 复制和 RNA 合成,并破坏 DNA 结构,最终导致肿瘤细胞死亡。此外,BL-B01D1 抗体部分的 Fc 段可以介导抗体依赖性的细胞毒作用,发挥杀伤肿瘤的作用。在癌症患者来源的肿瘤异种移植模型(源自肺癌、结肠癌、胰腺癌等)中,双特异性 ADC 药物 BL-B01D1 表现出比任何靶向 EGFR 或 HER3 的单一 ADC 药物更强的抗肿瘤效果。此外,Ma 等人先前发表的 I 期剂量递增和剂量扩展研究中已观察到其安全性和抗肿瘤活性的初步数据。此外,还建议将 II 期剂量 (RP2D) 设定为每 3 周第 1 天和第 8 天各一次,每次 2.5 mg kg-1,用于治疗晚期实体瘤。
由于食管鳞状细胞癌 (ESCC) 独特的解剖特征以及手术或疾病本身引起的并发症,其营养不良发生率较高且耐受性较差。该研究选择了两个剂量组(2.0 mg kg-1 和 2.5 mg kg-1),探讨 RP2D 对 ESCC 患者的适用性。作者展示了 BL-B01D1-103 研究(ClinicalTrials.gov 注册号:NCT05262491)剂量扩展阶段中 BL-B01D1 对既往接受过治疗的转移性 ESCC 患者的安全性、耐受性和有效性数据。这些数据为根据两个剂量组的结果确定 ESCC 患者的 RP2D 提供了依据。
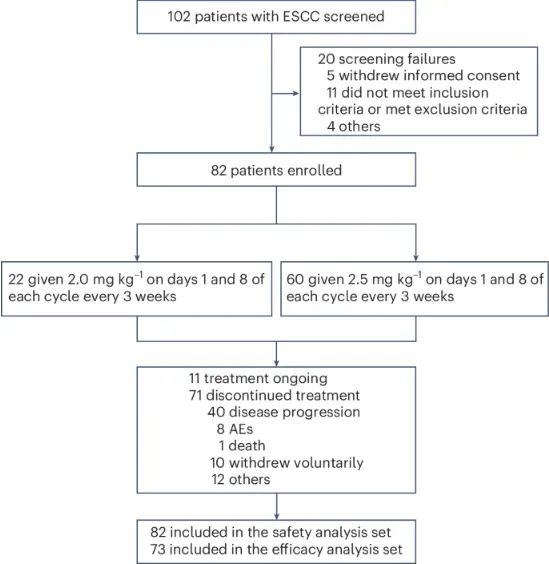
图1 CONSORT图(图源自Nature Medicine)
参考消息:
https://www.nature.com/articles/s41591-025-03792-7
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#食管鳞状细胞癌# #BL-B01D1#
3 举报