eGastroenterology:转甲状腺素蛋白淀粉样变性治疗进展
2025-07-24 eGastroenterology eGastroenterology 发表于上海
本文系统梳理了ATTR的发病机制、临床亚型、诊断策略与治疗进展,全面呈现了该领域近年来的重要突破,也为未来精准医疗的发展寄予了新期待。
导读
在医学界曾一度“沉默”的罕见病——转甲状腺素蛋白淀粉样变性(transthyretin amyloidosis, ATTR),迎来了前所未有的治疗曙光。近日,来自瑞典于默奥 (Umeå) 大学的Intissar Anan教授在eGastroenterology上发表了题为“Advances in the treatment of transthyretin amyloidosis”的综述文章,系统梳理了ATTR的发病机制、临床亚型、诊断策略与治疗进展,全面呈现了该领域近年来的重要突破,也为未来精准医疗的发展寄予了新期待。

背景介绍
ATTR是一种由于转甲状腺素蛋白(transthyretin, TTR)结构不稳定,形成淀粉样纤维沉积于体内多器官的疾病。TTR主要由肝脏合成,具有转运甲状腺素(T4)和维生素A结合蛋白的功能。正常情况下,TTR以四聚体形式稳定存在,当其解聚为单体后,会发生异常折叠,最终形成具有β折叠结构的淀粉样纤维,沉积于心肌、外周神经、胃肠道、肾脏甚至眼部等组织,引发器官功能障碍。
ATTR分为两大类,其病因、遗传特征及临床表型存在明显差异:
-
遗传性ATTR(hereditary ATTR, ATTRv):由TTR基因突变引起,常以外周神经病和心肌病起病,遗传方式为常染色体显性遗传;
-
野生型ATTR(wild type ATTR, ATTRwt):又称“老年性系统性淀粉样变性”,多见于65岁以上男性,无TTR基因突变,主要表现为心脏受累。
尽管ATTR长期被归类为“罕见病”,但随着影像技术与分子诊断方法的进步,其实际患病率可能被严重低估。统计数据显示,约13%的保留射血分数心衰(heart failure with preserved ejection fraction, HFpEF)患者及12%接受经导管主动脉瓣置换术(transcatheter aortic valve replacement, TAVR)的患者存在ATTR心肌病(ATTR with cardiomyopathy, ATTR-CM)。尸检研究发现,80岁以上男性中,高达25%存在ATTR。这一发现改变了人们对ATTR“罕见”的固有认知,提示其在老年群体中具有重要的公共卫生意义。
诊断进展:非侵入性影像与分子生物标志物联手破局
长期以来,ATTR诊断依赖于组织活检联合刚果红染色,该方法具有创伤性,且敏感性受限。近年来,非侵入性影像技术与生物标志物的快速发展,为该病的早期识别提供了新的可能。
-
骨显像(PYP/DPD/HMDP):若患者心肌摄取≥2级,且无单克隆蛋白证据,即可无创确诊ATTR-CM;
-
心脏磁共振(CMR):可显示广泛的延迟钆增强(late gadolinium enhancement, LGE)与T1/ECV值升高,为疑难病例的诊断提供强力支持;
-
神经丝轻链(NfL):ATTRv多发性神经病(ATTRv with polyneuropathy,ATTRv-PN)患者中,血液NfL水平与疾病严重程度及进展有关,未来有望用于疗效监测;
-
TTR基因检测:明确ATTRv与ATTRwt的类型,具有重要的临床与家系筛查意义。
药物治疗迎来“群雄逐鹿”
目前针对ATTR的治疗方式主要包括三大类:TTR稳定剂、基因沉默剂和抗淀粉样抗体。(见图1)
TTR稳定剂——防患于未“解聚”
-
Tafamidis(氯苯唑酸):Tafamidis通过稳定TTR四聚体,防止其解聚,适用于ATTRv-CM和ATTRwt-CM。ATTRACT临床试验证实,该药可显著降低全因死亡率和心源性住院率,并改善生活质量。Tafamidis已获得FDA与EMA批准,用于ATTR-CM患者,是首个被证实可改变疾病进程的药物。
-
Diflunisal(二氟尼柳):尽管Diflunisal属于非甾体抗炎药类药物,但亦可稳定TTR四聚体结构,多项观察性研究提示其对神经及心脏功能具有潜在益处,但因其药物不良反应限制了其在临床中的广泛应用。
基因沉默剂——从源头切断TTR表达
-
Patisiran(siRNA)与Inotersen(ASO):两者已获批用于治疗ATTRv-PN,研究显示,该药物可显著缓解神经症状并改善生活质量。
-
Vutrisiran:为新一代siRNA药物,以每季度一次皮下注射的方式给药,简化了治疗流程,HELIOS-B研究证实其在ATTR-CM患者中具有疗效,促使FDA于2025年批准其适应症拓展至ATTR-CM。
-
Eplontersen:是一种靶向肝细胞受体的反义寡核苷酸药物(antisense oligonucleotide, ASO),兼具疗效与安全性,NeuroTTRansform研究显示,该药物可改善神经症状并延缓疾病进展。
小知识:什么是siRNA和ASO药物?
siRNA是一种双链RNA分子,长度约为20–25个核苷酸,通过“RNA干扰(RNAi)”机制来选择性地降解目标mRNA,从而抑制特定蛋白的合成。其作用机制如下:
-
siRNA进入细胞后被载入RNA诱导沉默复合物(RISC);
-
RISC识别并切割与siRNA互补的TTR mRNA;
-
被切割的mRNA无法翻译,TTR蛋白生成减少;
-
适用于通过抑制肝脏合成TTR蛋白,治疗ATTR。
ASO是一种短单链DNA或RNA片段(15–25个核苷酸),可特异性地与目标mRNA结合,从而阻断其表达。其作用机制如下:
-
ASO与TTR mRNA互补结合形成双链;
-
激活核酸酶(如RNase H)降解该mRNA;
-
或通过阻断mRNA翻译过程,减少TTR蛋白生成,最终达到治疗ATTRv的目的。
抗淀粉样抗体——“拆除”沉积物
新型单克隆抗体(如PRX004、NI301A等)正试图通过直接清除淀粉样沉积物来实现治疗目的。PRX004在I期试验中已显示出改善心功能与神经评分的潜力,目前相关药物正处于II期研究阶段。
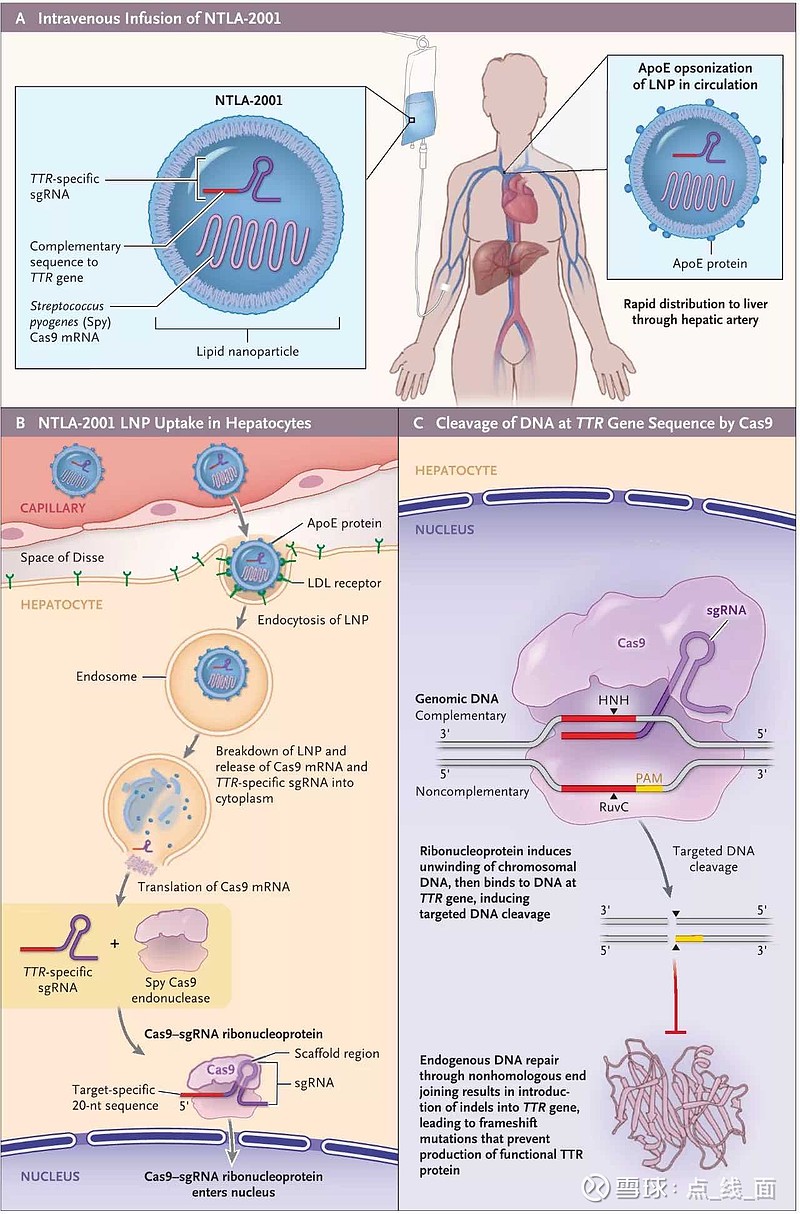
此外,CRISPR/Cas9基因编辑技术亦被引入ATTR的治疗探索中。NTLA-2001作为全球首个体内CRISPR疗法,通过单次静脉注射即可实现对TTR表达的长期抑制。在初期临床试验中,该药物展现出良好的安全性与持久疗效,标志着基因治疗进入新纪元。
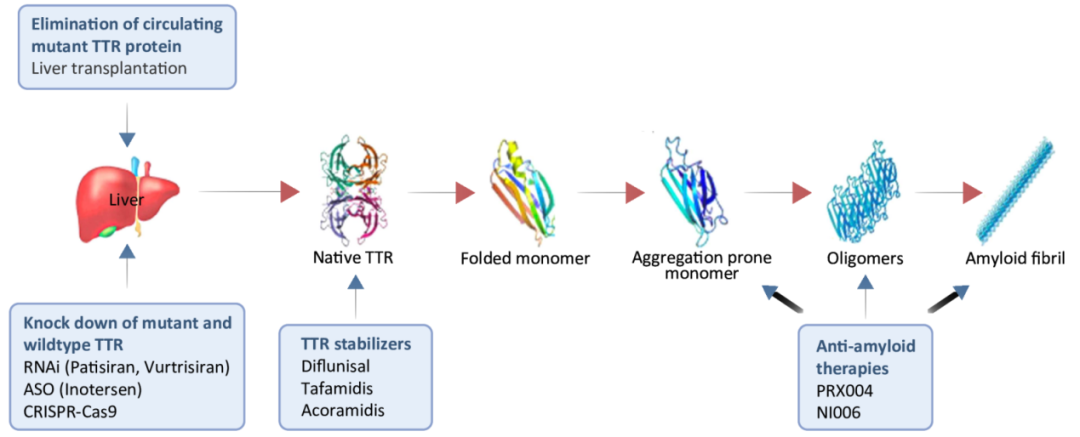
图1:针对ATTR基本发病机制的药物治疗策略。该图展现了TTR蛋白解聚、错误折叠和聚集等的一系列过程,最终导致淀粉样纤维的形成。重点介绍了治疗ATTRv的各种治疗方法和现有药物疗法。缩略语:ASO,反义寡核苷酸;ATTRv,遗传性转甲状腺素淀粉样变性;RNAi,RNA干扰;TTR,转甲状腺素
未来展望:向“精准医学”迈进
尽管治疗选择日益丰富,多个核心问题仍亟待解决:
(1)不同药物间的疗效与安全性缺乏对比研究;
(2)治疗顺序及联合策略尚无指南支持;
(3)治疗成本高昂、药物可及性受限;
(4)晚期器官损伤往往难以逆转;
(5)预防性治疗是否适用于无症状基因携带者尚无定论。
综上所述,ATTR正逐步从一个“冷门罕见病”走向聚光灯下。早期筛查、非侵入性诊断、生物标志物监测、靶向药物治疗和基因技术齐头并进,让患者从“束手无策”转变为“可防可治”。正如作者Anan教授在文中总结:“随着对ATTR发病机制的深入理解与治疗管线的不断拓展,为延缓发病、阻止进展、最终维持器官功能和生活质量带来了新希望。”
面对这样一种复杂但可控的疾病,学术界、产业界与公共卫生体系的多方协作,将是推动其疾病管理模式革新、实现“精准可及治疗”的关键。
引证本文
Intissar Anan - Advances in the treatment of transthyretin amyloidosis: eGastroenterology 2025;3:e100198.
https://doi.org/10.1136/egastro-2025-100198

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#转甲状腺素蛋白淀粉样变性#
15 举报