重庆医科大学蒋宁团队《AFM》:靶向递送 CRISPR-Cas9 和 ACC 抑制剂的智能纳米笼有效增强抗肿瘤级联治疗
2025-01-23 BioMed科技 BioMed科技 发表于陕西省
全球癌症患者多、死亡率高,现有疗法效果有限。重庆医科大学蒋宁团队开发双层响应纳米载体,同时装载 CRISPR - Cas9 和抑制剂,双重抑制 ACC1,展现显著抗肿瘤效果。
全球每年新增恶性肿瘤患者 2000 万,近 970 万人因此死亡。纵使临床治疗手段丰富,包括手术、化疗、放疗等传统方法和靶向、免疫等新型疗法,但治疗效果仍然有限。因此,亟需开发更安全有效的治疗方案,改善癌症患者预后。
最近,重庆医科大学基础医学院蒋宁团队开发出一种创新性肿瘤治疗方案,为癌症治疗带来新希望。该团队巧妙设计了双层响应型纳米载体系统,通过同时装载基因编辑工具(CRISPR-Cas9)和小分子抑制剂(ND630),精准靶向肿瘤细胞。这种智能载体系统能够响应肿瘤微环境,释放药物,双重抑制脂质代谢关键蛋白ACC1。研究发现,该治疗方案可显著增加肿瘤细胞对多不饱和脂肪酸(PUFA)的摄取,触发脂质过氧化反应,最终通过铁死亡和细胞凋亡等多种途径导致肿瘤细胞死亡,展现出显著的抗肿瘤效果。重庆医科大学研究生赵薇、张腊、郭焦为该论文的共同第一作者,重庆医科大学基础医学院蒋宁副教授为唯一通讯作者,文章发表在Advanced Functional Materials杂志上。
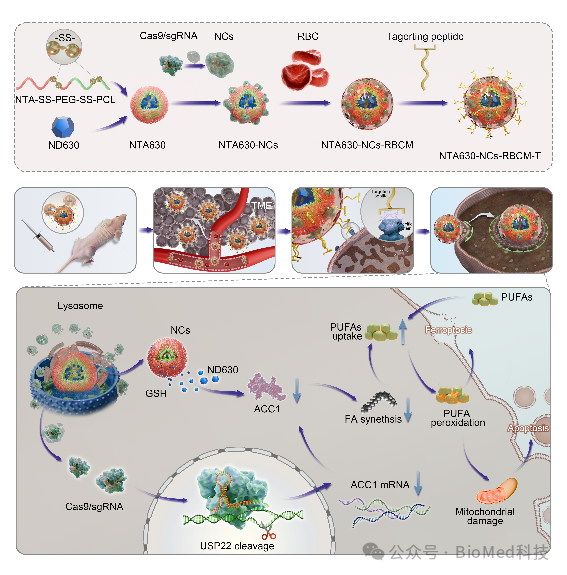
图1:双层响应型载药纳米笼合成步骤示意图
该科研团队成功研发了一种名为NTA630-NCs-RBCM-T的新型纳米载药系统。在制备过程中,首先通过纳米自沉淀法将ACC抑制剂包裹形成NTA630胶束;同时,利用原位自由基聚合技术将Cas9与sgRNA复合物包裹,制备出具有阳离子和酸响应性的可降解纳米胶囊(NC)。随后,通过静电吸附将NCs与NTA630结合形成NTA630-NCs,再将其包裹在红细胞膜中并与GPC3靶向肽共孵育,最终得到具有靶向性的NTA630-NCs-RBCM-T纳米载体(如图1所示)。
研究团队通过CCK8实验、生物透射电镜和活死染色等多种方法验证了该纳米载体的抗肿瘤效果。实验结果表明,这种多功能纳米载体在到达肿瘤细胞后,在溶酶体中红细胞膜被降解后,ND630得以释放,并在酸性环境下释放Cas9复合物,最终有效诱导肿瘤细胞死亡。
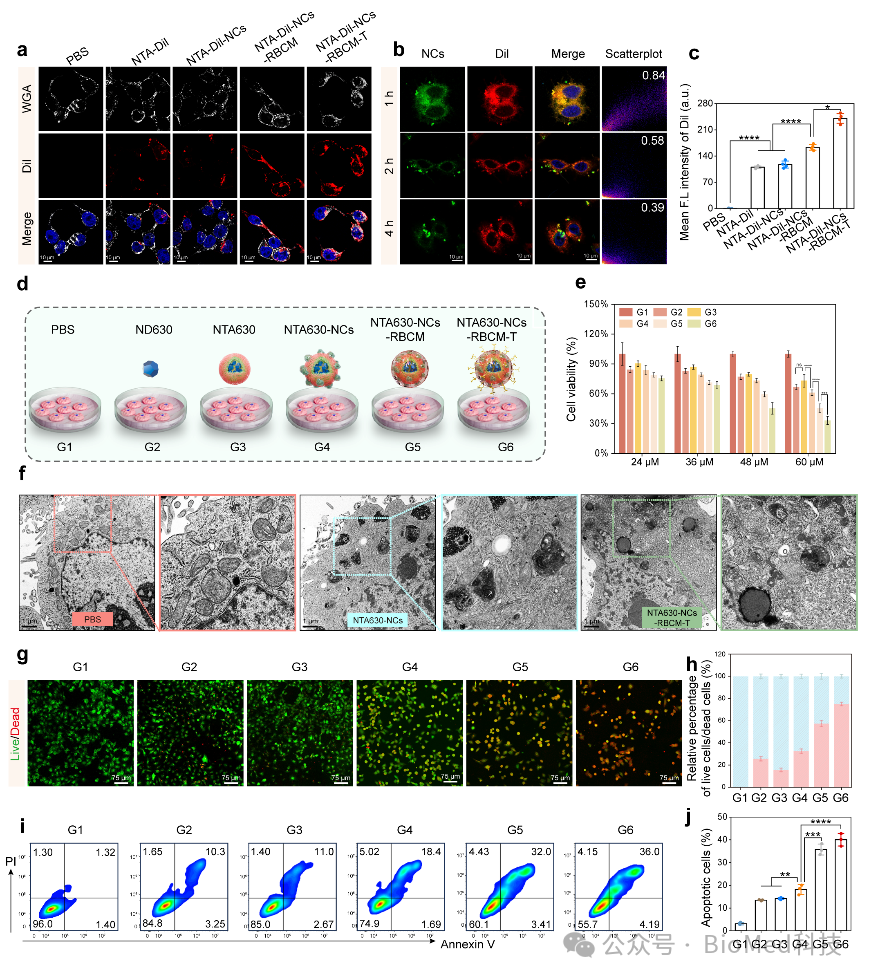
图2:双层响应型载药纳米笼对肿瘤杀伤作用的验证
为探究 NTA630-NCs-RBCM-T 抑制癌细胞增殖的分子机制,研究团队进行脂代谢组学分析,结果显示,NTA630-NCs-RBCM-T能够有效抑制脂肪酸合成途径,不仅导致饱和脂肪酸显著减少,还促进了细胞对多不饱和脂肪酸(PUFA)的摄取。由于PUFA极易发生过氧化反应,这一过程最终加速了癌细胞的死亡(如图3所示)。
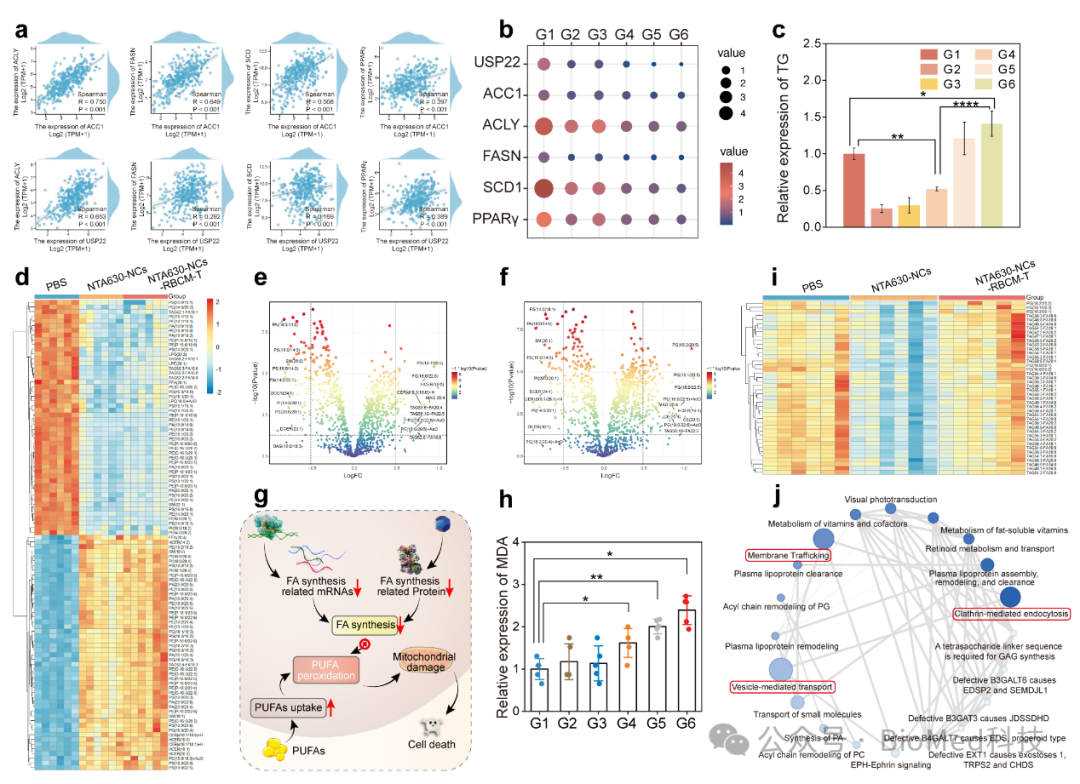
图3:双层响应型载药纳米笼靶向脂质代谢的验证
进一步在动物实验中验证 NTA630-NCs-RBCM-T NPs 的抗肿瘤作用。首先利用动物活体荧光成像研究NTA630-NCs-RBCM-T NPs ,证实其对肿瘤的靶向作用;再通过对小鼠体重、肿瘤大小、生存时间的观察记录以及肿瘤的 Ki-67,TUNEL 染色,结果明确NTA630-NCs-RBCM-T NPs 的体内抗肿瘤作用显著(如图4所示)。
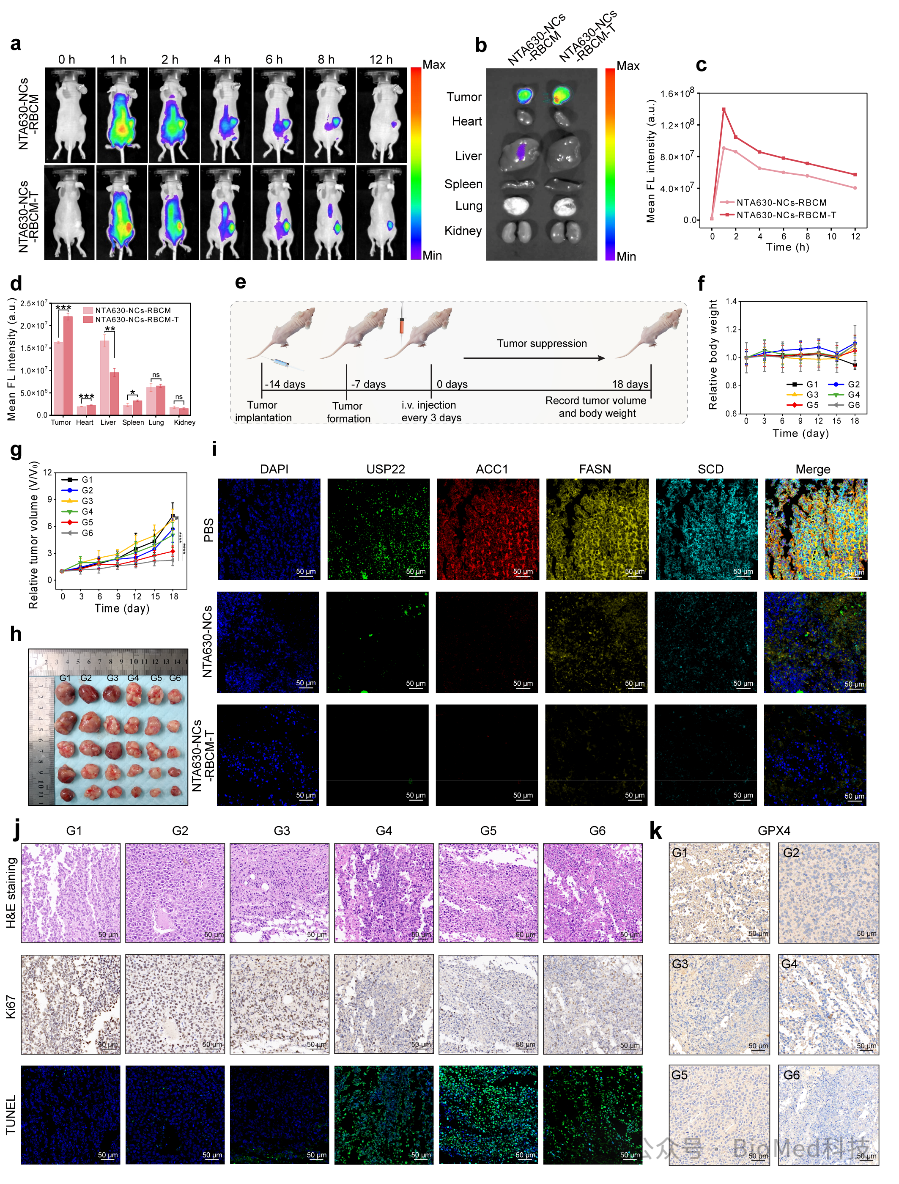
图4:双层响应型载药纳米笼的体内抗肿瘤效果评估
基于上述结果,在这项研究中,我们开发了一种由红细胞膜封装的纳米笼,称为 NTA630-NCs-RBCM-T,旨在共同递送 CRISPR-Cas9 和 ACC 抑制剂。这种创新方法促进了双靶点 ACC 抑制,增强了级联抗癌治疗的疗效。该研究在遗传和代谢水平上实现了对肿瘤细胞的双重攻击,显着改善了治疗结果。未来,这种双负载纳米笼技术可以通过改变靶向肽来适应,使其可以应用于其他类型的肿瘤或疾病。
参考文献:
W. Zhao, L. Zhang, J. Guo, Q. Xu, M. Zhang, H. Liu, C. Ren, Y. Zhao, J. Wang, Q. Peng, N. Jiang, Intelligent Nano-Cage for Precision Delivery of CRISPR-Cas9 and ACC Inhibitors to Enhance Antitumor Cascade Therapy Through Lipid Metabolism Disruption. Adv. Funct. Mater. 2025, 2418090.
https://doi.org/10.1002/adfm.202418090
原文链接:
https://advanced.onlinelibrary.wiley.com/doi/full/10.1002/adfm.202418090
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#CRISPR-Cas9# #纳米载体#
0 举报