Eur Heart J 北京大学冼勋德课题组揭示KIF13B调控胞葬功能:破解非血脂依赖性动脉粥样硬化新密码
6小时前 论道心血管 论道心血管 发表于上海
这一发现不仅深化了对动脉粥样硬化复杂病理机制的理解,还为开发针对该疾病的新型治疗靶点提供了重要依据。
动脉粥样硬化是引发心脑血管疾病的主要原因,尽管他汀类药物和PCSK9抑制剂等降脂疗法在过去几十年中显著降低了患者血脂水平,但动脉粥样硬化性心血管病(ASCVD)的残余风险依然逐年攀升。这提示,动脉粥样硬化的病理机制远超血脂异常,亟需挖掘更精准的分子靶点。
2025年7月25日,由北京大学冼勋德课题组领衔,在世界著名期刊European Heart Journal杂志上发表了题为“The macrophage-derived motor protein KIF13B enhances MERTK-mediated efferocytosis and prevents atherosclerosis in mice”的文章,为ASCVD的治疗开辟了全新路径,揭示了KIF13B通过调控巨噬细胞的胞葬功能(efferocytosis)在动脉粥样硬化发生和发展中的关键作用。这一发现不仅深化了对动脉粥样硬化复杂病理机制的理解,还为开发针对该疾病的新型治疗靶点提供了重要依据。

冼勋德课题组的本次研究聚焦于Kinesin家族最大成员KIF13B。此前,该课题组已证实KIF13B在肝脏脂质代谢和代谢相关脂肪肝(MAFLD)中发挥重要作用,但其在动脉粥样硬化中的功能尚属未知。该研究发现,在动脉粥样硬化患者的动脉组织中,KIF13B表达水平显著下降,且在高脂饮食诱导的低密度脂蛋白受体敲除(Ldlr-/-)小鼠模型中,其表达量与疾病严重程度呈负相关。通过全身敲除、巨噬细胞特异性敲除Kif13b基因,以及Kif13b缺陷骨髓移植实验,均观察到动脉粥样硬化斑块面积显著增大,巨噬细胞浸润加剧,斑块内细胞凋亡增加,且这些病理变化与血浆脂质水平无关。这一发现表明,KIF13B在动脉粥样硬化中的作用独立于传统降脂机制。
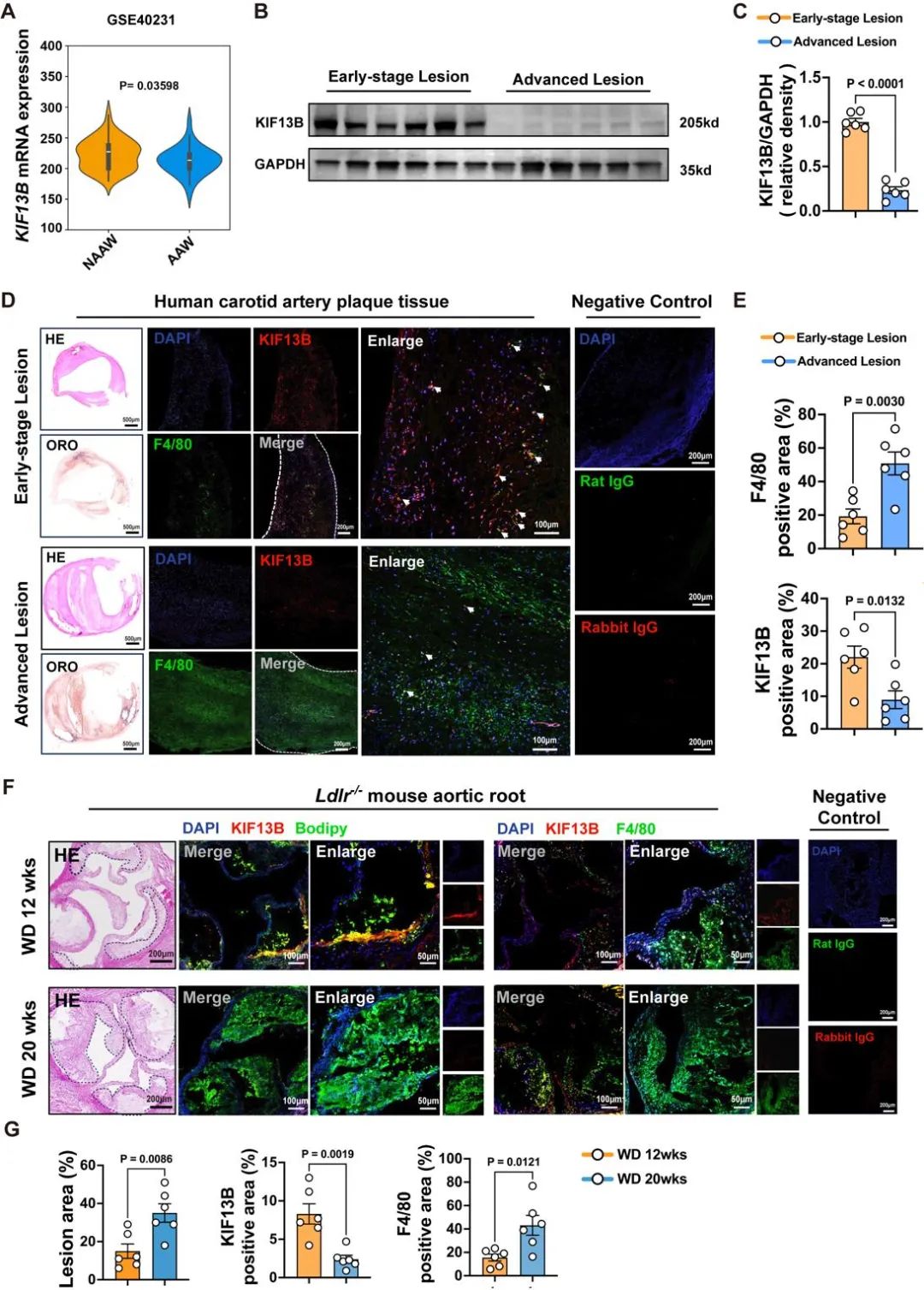
结果1:KIF13B的表达与患者和小鼠动脉粥样硬化的进展呈负相关
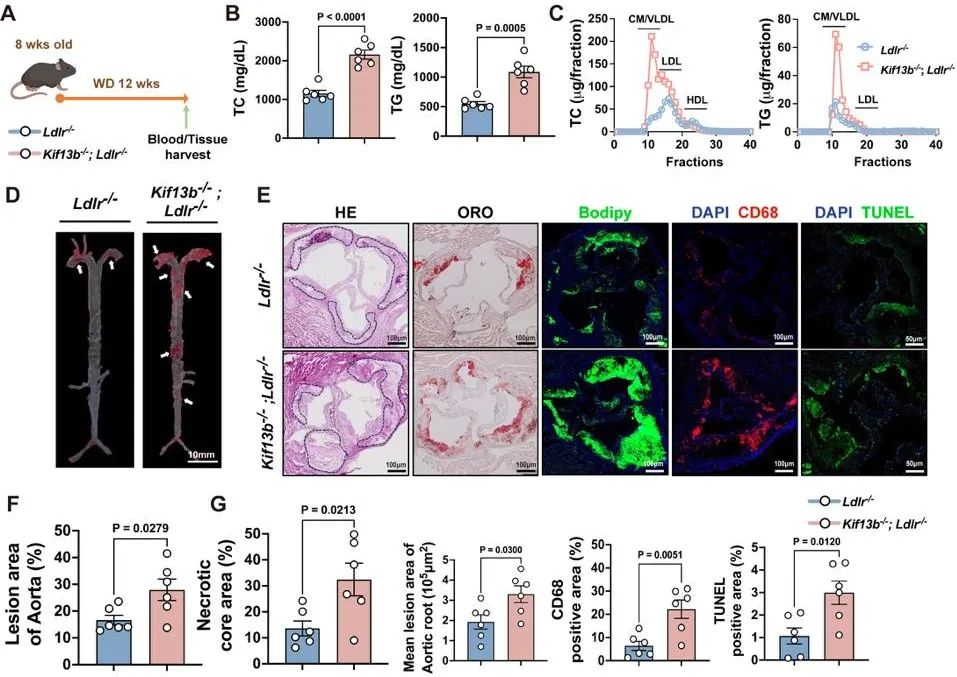
结果2:Ldlr-/-小鼠Kif13b的缺失会加剧动脉粥样硬化
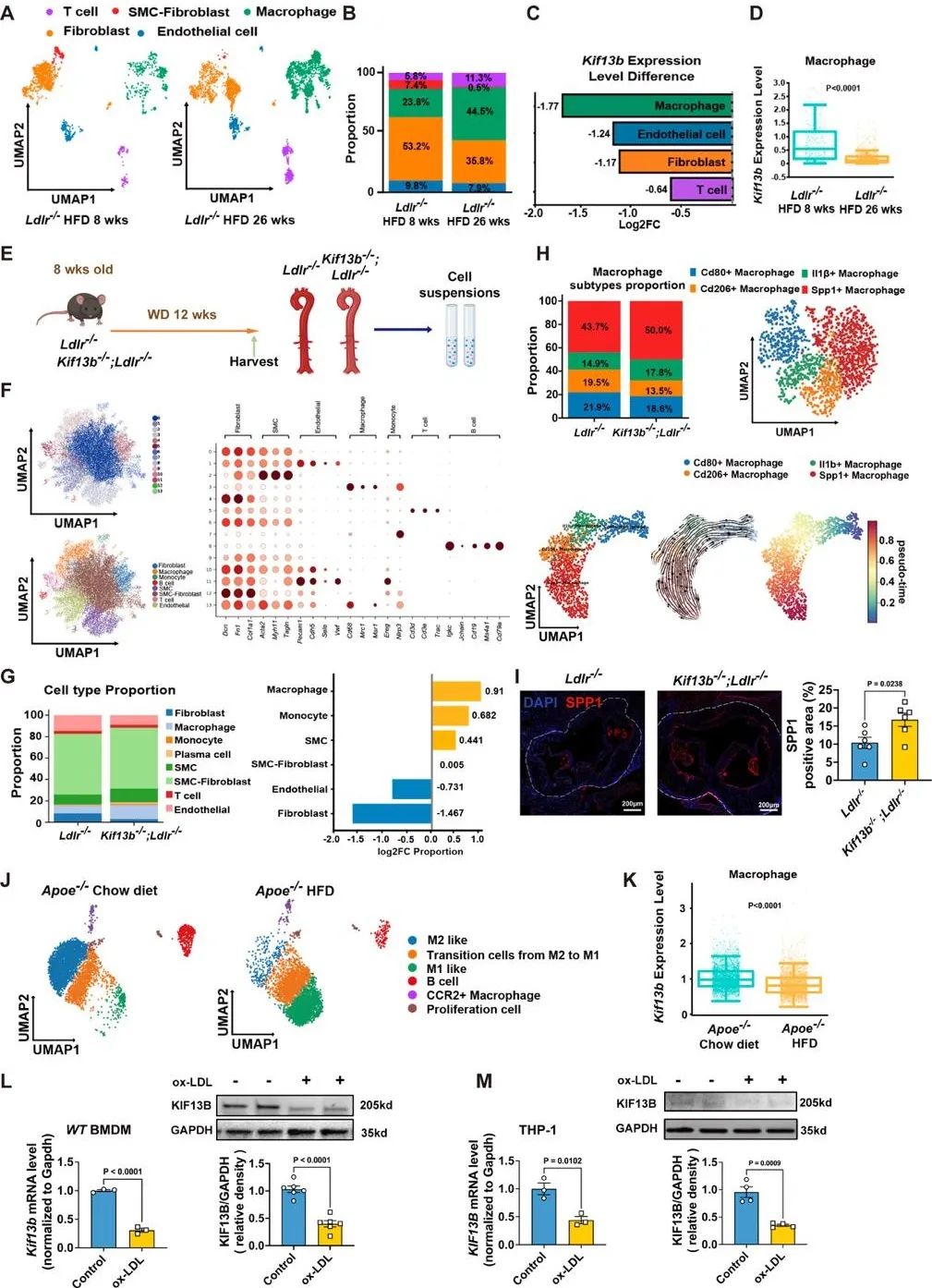
结果3:Kif13b缺乏主要影响小鼠动脉粥样硬化中的巨噬细胞动力学
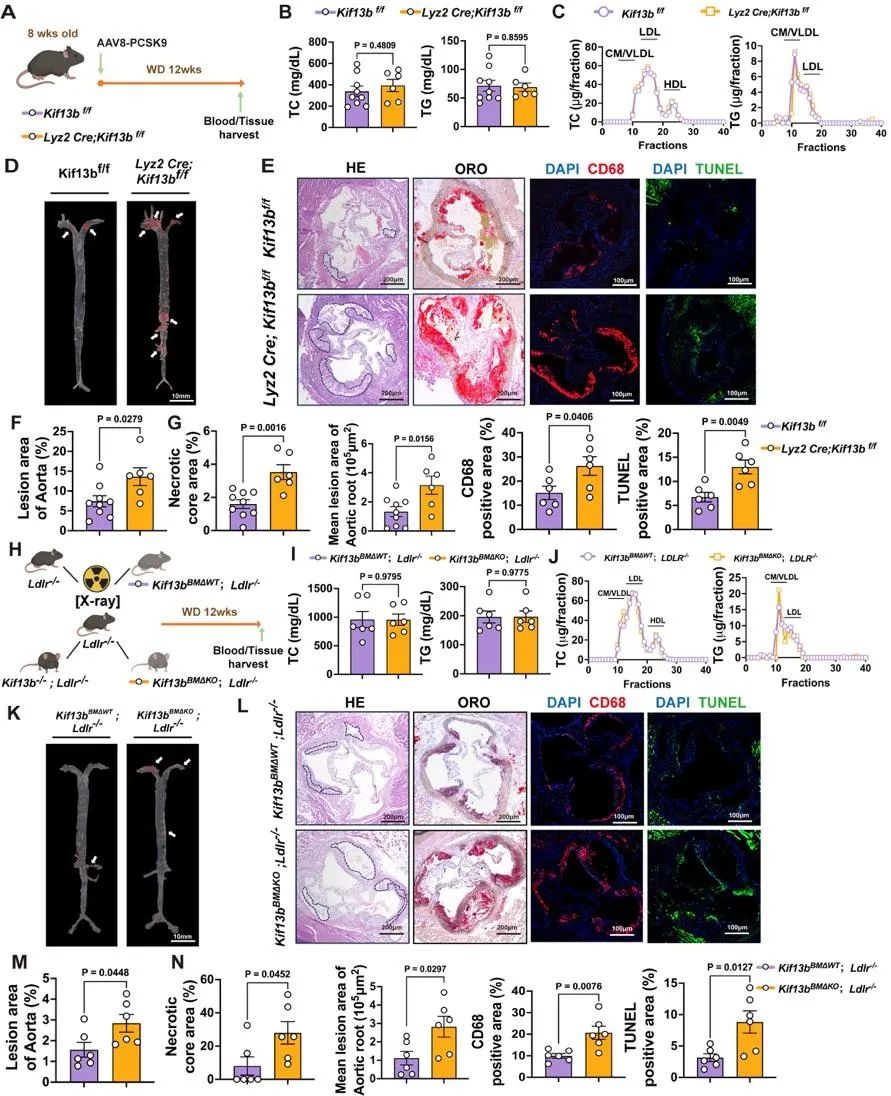
结果4:Kif13b的髓系特异性缺失以非脂质依赖的方式加重动脉粥样硬化
进一步的机制研究揭示,KIF13B通过KIF13B-ITCH-CBL-MERTK信号轴调控巨噬细胞的胞葬功能。胞葬是巨噬细胞清除凋亡细胞的过程,其功能障碍是动脉粥样硬化斑块进展的核心环节。而该研究发现,Kif13b缺失导致E3泛素连接酶ITCH表达下调,进而增强CBL介导的MERTK蛋白泛素化降解,显著削弱巨噬细胞的胞葬能力。MERTK作为关键的胞葬受体,其表达减少直接加剧了斑块的炎症和不稳定性。
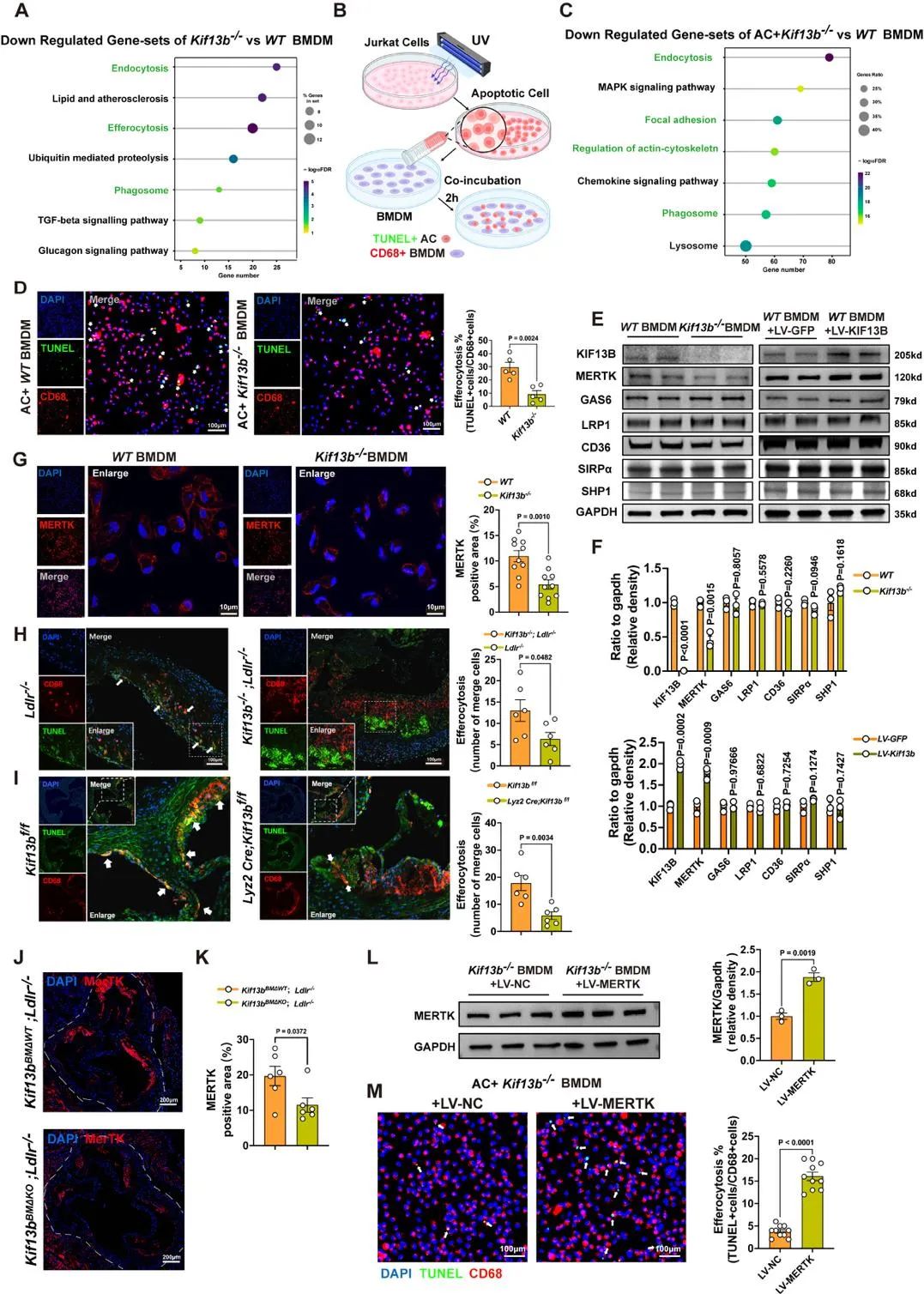
结果5:Kif13b的缺失抑制了MERTK介导的巨噬细胞的胞葬作用
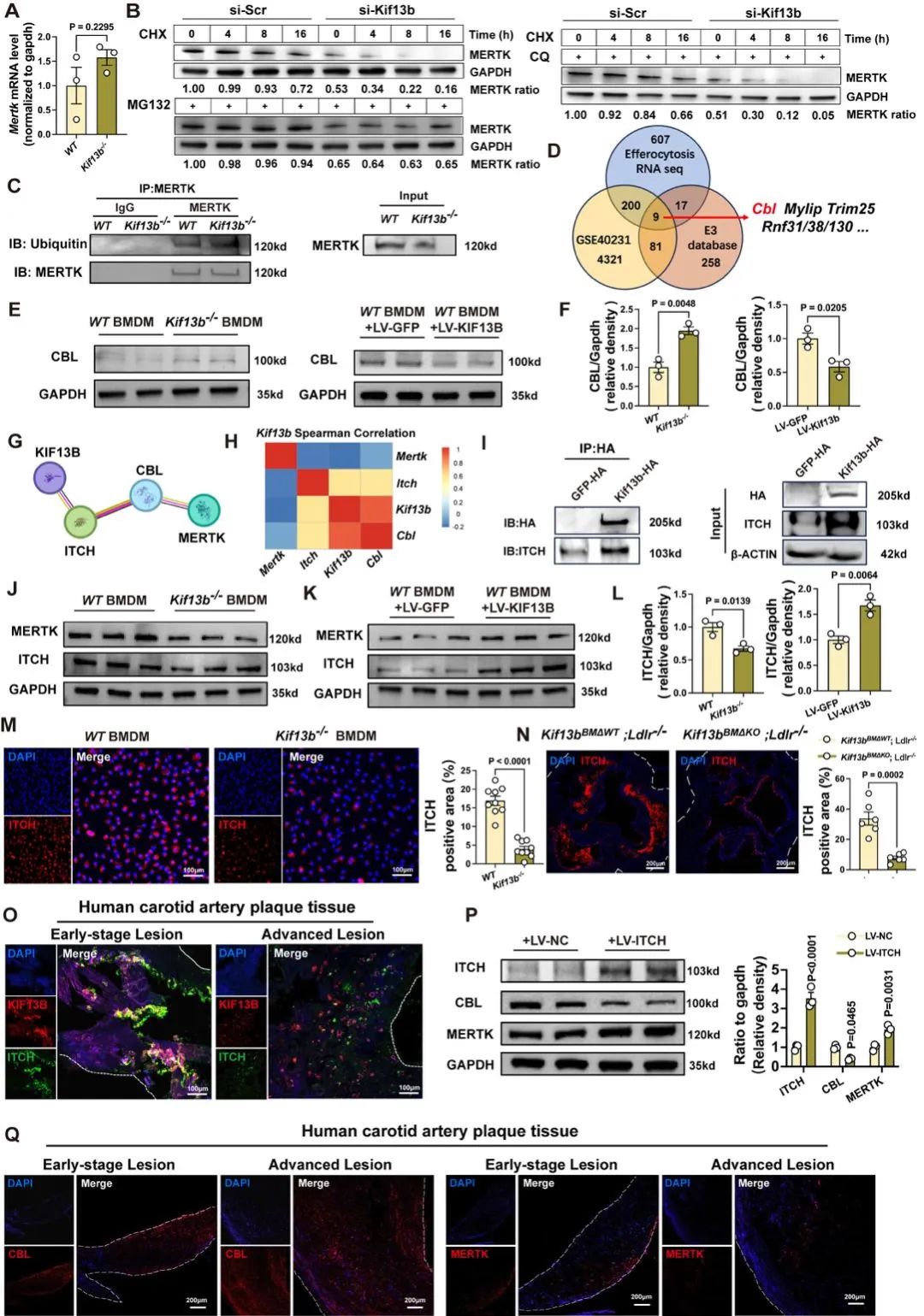
结果6:KIF13B通过与巨噬细胞中的ITCH相互作用,减少CBL介导的MERTK泛素化
更令人振奋的是,冼勋德团队测试了一种正处于I期临床试验的CBL抑制剂NX1607,发现其能显著恢复MERTK蛋白水平,增强巨噬细胞的胞葬功能,从而在Kif13b缺失小鼠中有效抑制动脉粥样硬化病变的发展。这一疗效不依赖于血脂降低,且未观察到明显副作用,提示NX1607可能成为针对血脂水平正常但仍患有动脉粥样硬化患者的全新治疗策略。目前该项专利(CBL抑制剂NX1607在制备治疗动脉粥样硬化药物中的应用)已获批。
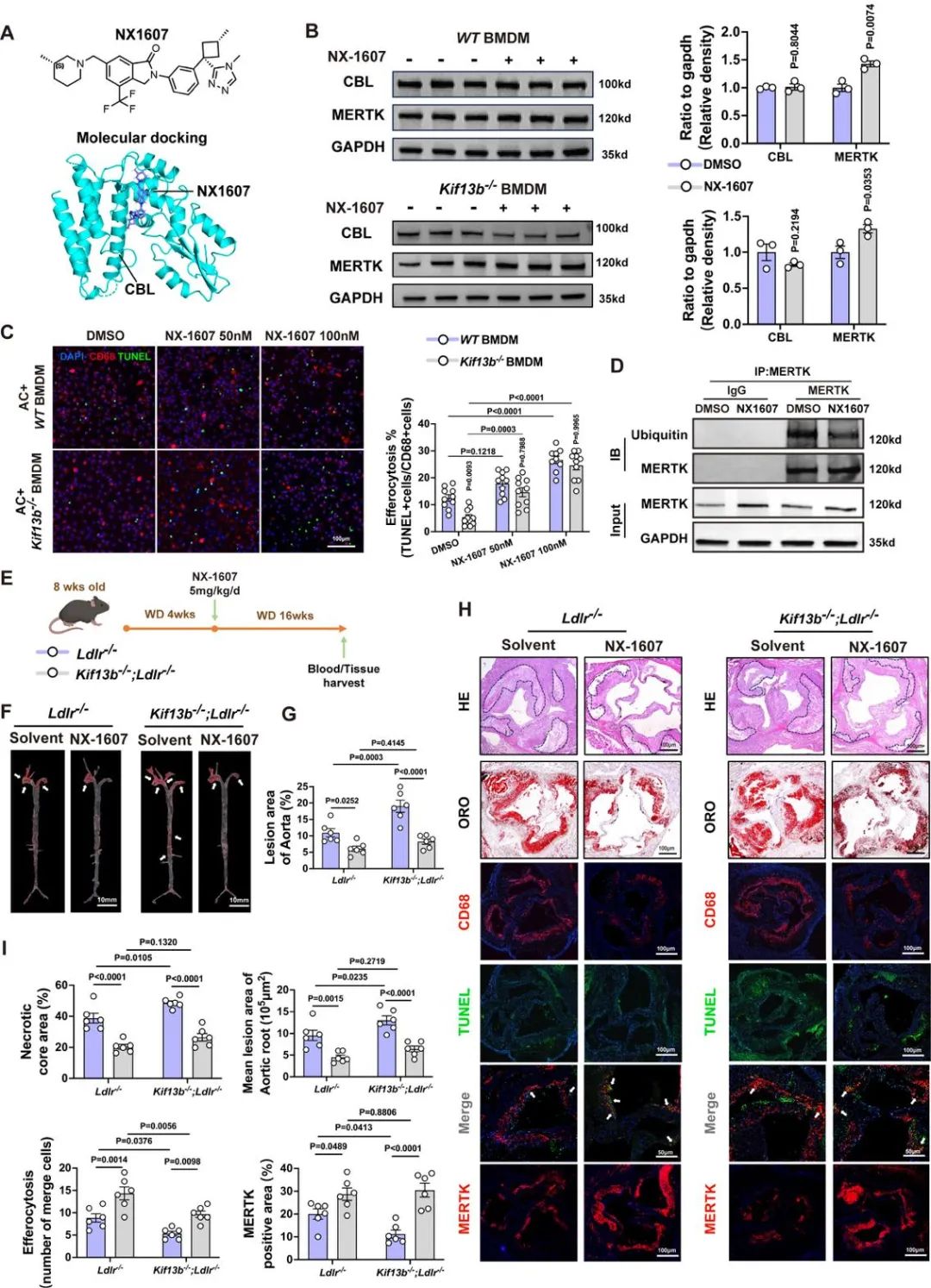
结果7:CBL抑制剂NX-1607通过增强巨噬细胞的胞葬功能,有效地改善了动脉粥样硬化
综上,该研究通过揭示KIF13B在胞葬功能和动脉粥样硬化中的核心作用,为这一疾病的精准治疗提供了新视角。KIF13B作为潜在治疗靶点的发现,不仅丰富了动脉粥样硬化病理机制的理论框架,也为开发新型药物提供了坚实基础。课题组表示,NX1607的临床试验进展值得期待,其可能推动针对ASCVD的创新疗法早日应用于临床,造福全球患者。
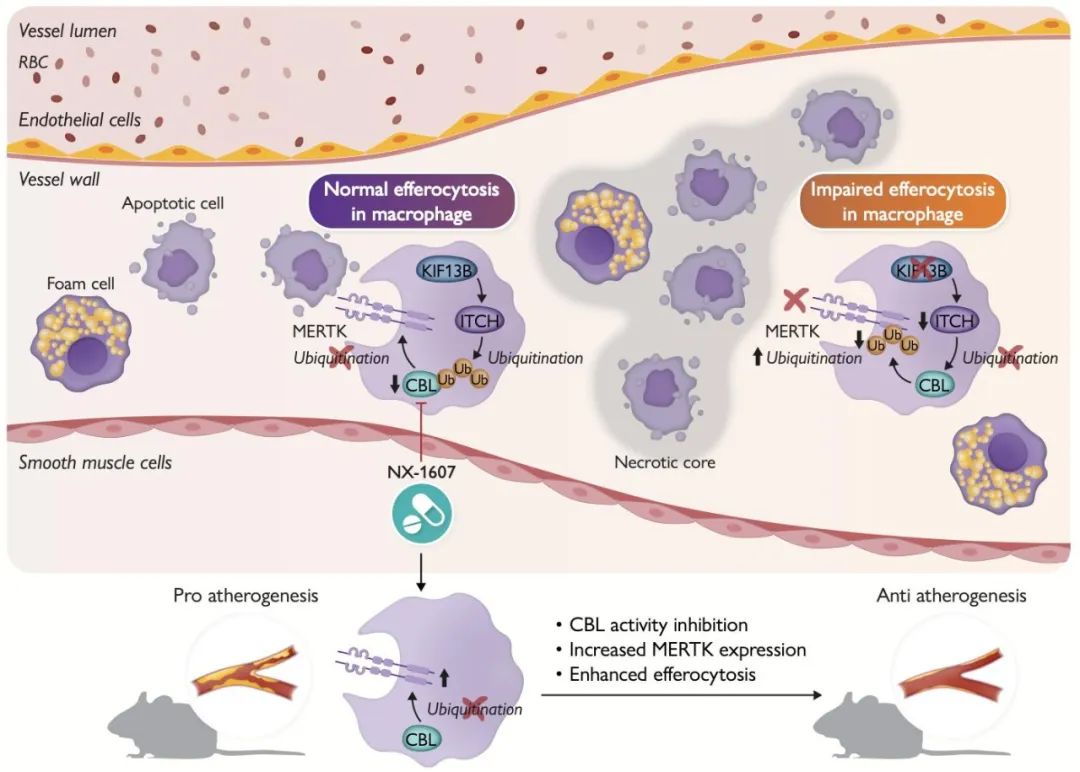
总而言之,这一发现的意义在于,它不仅破解了KIF13B在动脉粥样硬化中的“分子密码”,还通过调控胞葬功能为心血管疾病的治疗提供了全新思路。未来,随着冼勋德课题组对KIF13B相关研究的深入,动脉粥样硬化的防治有望迎来新的突破。
北京大学心血管研究所冼勋德研究员、基础医学院医学生物信息学系赵东宇研究员与郑州大学第一附属医院唐俊楠教授为本文共同通讯作者。北京大学博士生徐一童、陈婧璇、刘一冉、郑州大学第一附属医院博士生张格、北京大学第三医院博士后苗国琳、北京大学博士后吴靖东为本文的共同第一作者。本研究得到北京大学心血管研究所董尔丹院士、黄薇副教授、王宇辉副研究员以及北京大学临床医学高等研究院赵扬研究员的帮助,受到国家自然科学基金委、北京市自然科学基金委和血管稳态与重构全国重点实验室的大力支持。
原文链接:
https://doi.org/10.1093/eurheartj/ehaf523
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言


















前往app查看评论内容
3 0 举报