Molecular Neurodegeneration:脂肪间充质干细胞联合类淋巴系统激活对朊病毒病的协同治疗作用
2025-04-22 xiongjy MedSci原创
本研究证实AdMSCs与可乐定联合治疗可显著延长ME7朊病毒感染小鼠生存期至373天(未治疗组230.7天)。
朊病毒病作为一类由朊蛋白(PrP)构象异常导致的致死性神经退行性疾病,目前临床尚缺乏有效治疗手段。该研究创新性地提出将脂肪来源间充质干细胞(AdMSCs)移植与类淋巴系统激活药物可乐定联合应用的策略,通过多机制协同作用实现对朊病毒病的干预。

研究团队首先从6-8周龄C57BL/6J小鼠腹股沟脂肪组织中分离培养AdMSCs,并通过三系分化潜能和表面标志物(CD29、CD44、Sca-1阳性率>95%)验证其干细胞特性。实验采用ME7朊病毒株感染模型,在感染后7天开始每周腹腔注射可乐定(100μg/kg),并于感染后70天实施单次颅内AdMSCs移植(1×10^5细胞/30μL)。值得注意的是,联合治疗组小鼠在长达373天的观察期内未出现典型朊病毒病症状,生存期较未治疗组(230.7±1.4天)显著延长(p<0.0001),这是迄今报道中朊病毒病模型最显著的生存获益。
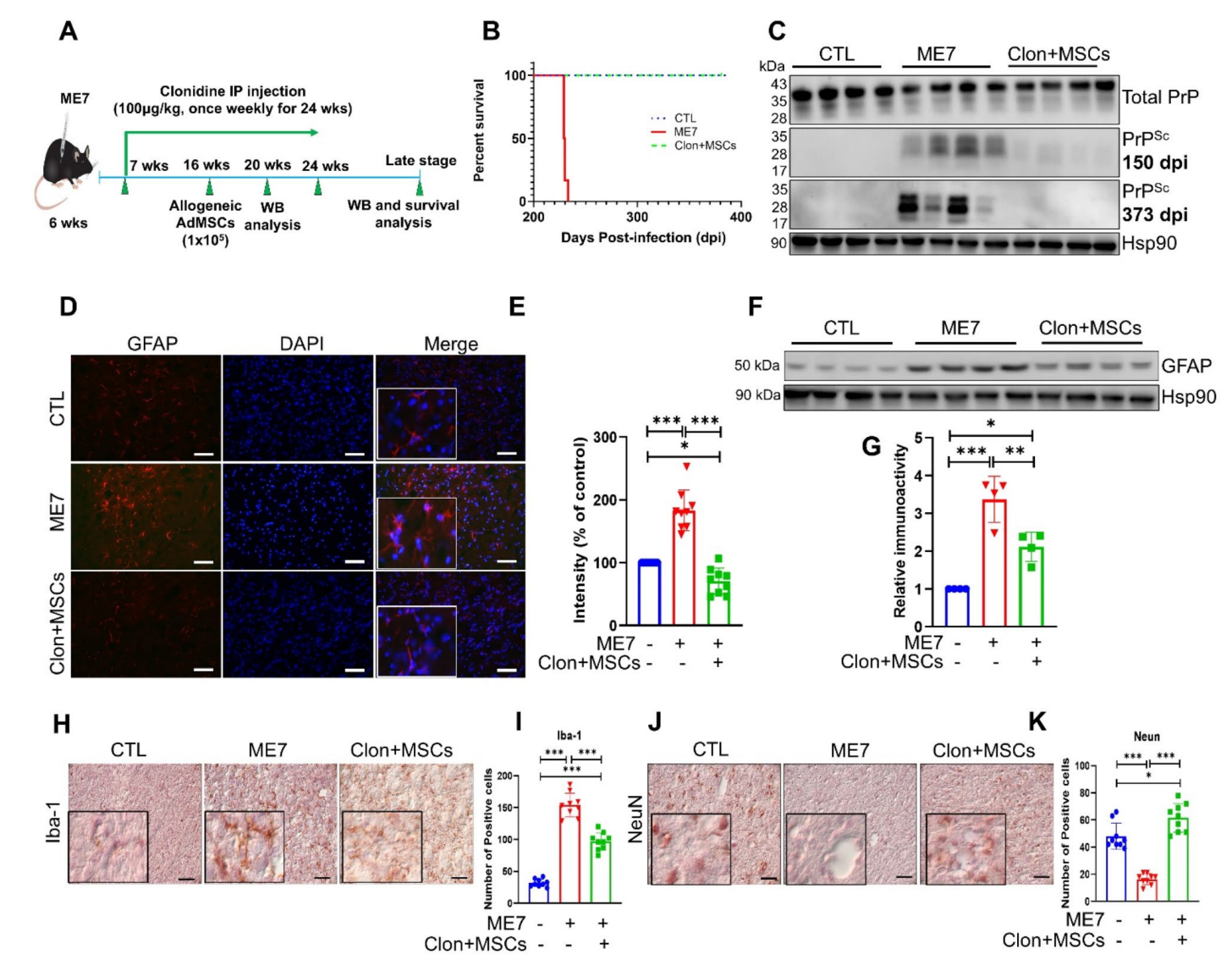
图1:实验设计与治疗效果
在分子机制层面,Western blot分析显示联合治疗可特异性降低脑组织PrP^Sc沉积(150dpi时减少约65%),而不影响总PrP表达,提示其通过促进错误折叠蛋白清除而非抑制正常朊蛋白合成发挥作用。免疫组化进一步证实,治疗组丘脑区域GFAP阳性星形胶质细胞密度降低72%(p<0.001),Iba-1阳性小胶质细胞减少68%(p<0.001),表明显著抑制了朊病毒特征性的神经炎症反应。尤为关键的是,NeuN免疫染色显示治疗组神经元存活率提高2.3倍(p<0.001),证实该方案具有神经保护作用。研究者推测其协同机制可能涉及:1)可乐定通过激活类淋巴系统增强PrP^Sc的脑脊液-淋巴引流;2)AdMSCs分泌神经营养因子(如BDNF、GDNF)抑制神经元凋亡;3)干细胞旁分泌作用调节神经免疫微环境。
该研究首次证实靶向类淋巴系统的药物与干细胞移植的协同效应,为朊病毒病这种难治性疾病提供了全新治疗范式。不过需注意的是,不同朊病毒株(如RML、22L)可能存在治疗反应差异,且长期安全性有待验证。未来研究可优化给药方案(如可乐定剂量梯度、AdMSCs多次移植),并探索在阿尔茨海默病等其他蛋白错误折叠疾病中的应用潜力。
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











前往app查看评论内容
6 0
前往app查看评论内容
0 0