JHO:Olutasidenib 联合阿扎胞苷疗法显成效,复发难治性 mIDH1 AML 的新治疗选择
8小时前 吾乃喵大人 MedSci原创 发表于上海
本研究系统评估了Olutasidenib联合阿扎胞苷治疗复发或难治性mIDH1 AML患者的临床疗效及安全性,显示了显著且持久的缓解与可控的毒副反应谱。
研究亮点
- Olutasidenib联合阿扎胞苷(OLU+AZA)在复发或难治性(R/R)突变IDH1急性髓系白血病(mIDH1 AML)患者中展现了31%的CR/CRh率与51%的整体反应率,缓解持续时间达14.7个月。
- 与既往接受过Olutasidenib单药治疗的患者相比,未接受该药的患者中反应率更高(CR/CRh达37%,ORR 59%),显示该组合治疗对既往未暴露患者具有更佳疗效。
- 联合治疗安全性良好,主要高等级不良事件为血小板减少(37%)、红细胞减少(25%)、中性粒细胞减少(24%),仅6%因不良事件中断治疗,显示良好耐受性。
近期,发表于Journal of Hematology & Oncology杂志的一项多中心开放标签Ⅰ/Ⅱ期临床试验,由国际专家团队联合开展,聚焦于评价口服选择性突变IDH1抑制剂olutasidenib联合标准HMA药物阿扎胞苷治疗复发或难治性mIDH1 AML患者的疗效和安全性。试验纳入67例患者,涵盖多种既往治疗史,系统分析了组合方案的缓解率、生存期及不良反应谱,为这一难治白血病亚组提供了潜在的新治疗选项。

急性髓系白血病(AML)是一种异质性极强的造血系统恶性肿瘤,其中约7-14%的患者存在IDH1基因突变。IDH1突变导致异常代谢产物D-2-羟基戊二酸(2-HG)大量积累,抑制细胞正常分化,促进白血病发生。因此,针对IDH1突变的靶向治疗已成为研发重点。尽管目前已有IDH1抑制剂(如ivosidenib和olutasidenib)获批,但复发难治患者(R/R AML)治疗仍面临反应率低、缓解持续时间短及耐药发生等问题。基于此,联合IDH1抑制剂与低强度化疗药物(如阿扎胞苷)的策略逐渐兴起,旨在增强疗效、延长缓解时间。
本临床试验融合了Ⅰ期剂量递增和Ⅱ期多队列扩展设计,纳入≥18岁证实的mIDH1 R/R AML患者。患者接受150 mg Olutasidenib每日两次口服联合标准剂量阿扎胞苷(75 mg/m²,7天),治疗周期28天重复。研究特别区分了既往接受过HMA和IDH1抑制剂治疗的患者群体。主要终点为CR/CRh率,次要终点包括整体反应率(ORR)、缓解持续时间、56天输血依赖性缓解及总生存期(OS)。持续跟踪不良事件(AE)发生情况,使用NCI-CTCAE 4.03标准分级。
研究结果
患者特征及治疗暴露
- 纳入患者67例,年龄中位数66岁(28-82岁),男性54%。
- 83%患者接受过≥2线既往治疗;40%既往接受过HMA,31%既往接受IDH1抑制剂治疗(其中24%接受过Olutasidenib单药治疗)。
- 10%经历过造血干细胞移植(HSCT)。
- 蛋白质型IDH1突变以R132C(60%)和R132H(28%)为主。
- 平均接受治疗周期5个(范围1-61)。
疗效表现
| 指标 | 全体患者 (N=67) | 排除既往Olutasidenib者(N=51) |
|---|---|---|
| CR率 | 27% (18/67) | 31% (16/51) |
| CR/CRh率 | 31% (21/67) | 37% (19/51) |
| ORR(≥PR) | 51% (34/67) | 59% (30/51) |
| CR中位持续时间 | 20.3个月 (95% CI 3.7-NR) | 20.3个月 (95% CI 5.6-NR) |
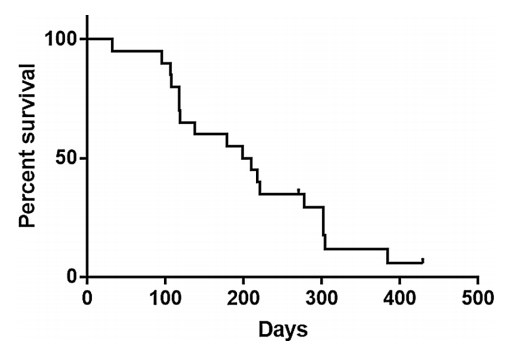
| CR/CRh中位持续时间 | 14.7个月 (95% CI 4.6-NR) | 14.7个月 (95% CI 4.6-NR) |
| 总生存中位时间 | 12.9个月 (95% CI 8.7-19.3) | 18.1个月(无既往Olutasidenib) |
(NR = 未达到)
- 响应出现的中位时间为约2-3个月。
- 12名实现缓解患者中,58%随后接受HSCT治疗。
- 剔除既往Olutasidenib暴露患者,疗效明显提升,显示组合疗法对首次使用者更具临床意义。
- 5名既往接受Ivosidenib患者中,2例实现CR,可见二线或三线治疗仍存在获益可能。
- 输血依赖患者中,CR/CRh患者分别有64%(RBC)和57%(血小板)实现56天以上输血独立(图3)。
安全性
- 97%患者发生至少1例治疗相关不良事件。
- 69%患者出现治疗相关不良事件。
- 主要≥3级不良事件包括血小板减少(37%)、红细胞减少(25%)、中性粒细胞减少(24%)。
- 9%发生分化综合症,其中大多数可通过剂量调整与对症治疗管理。
- 只有6%患者因不良事件中断治疗。
- 无因药物直接致死事件记录,死因多为疾病进展。
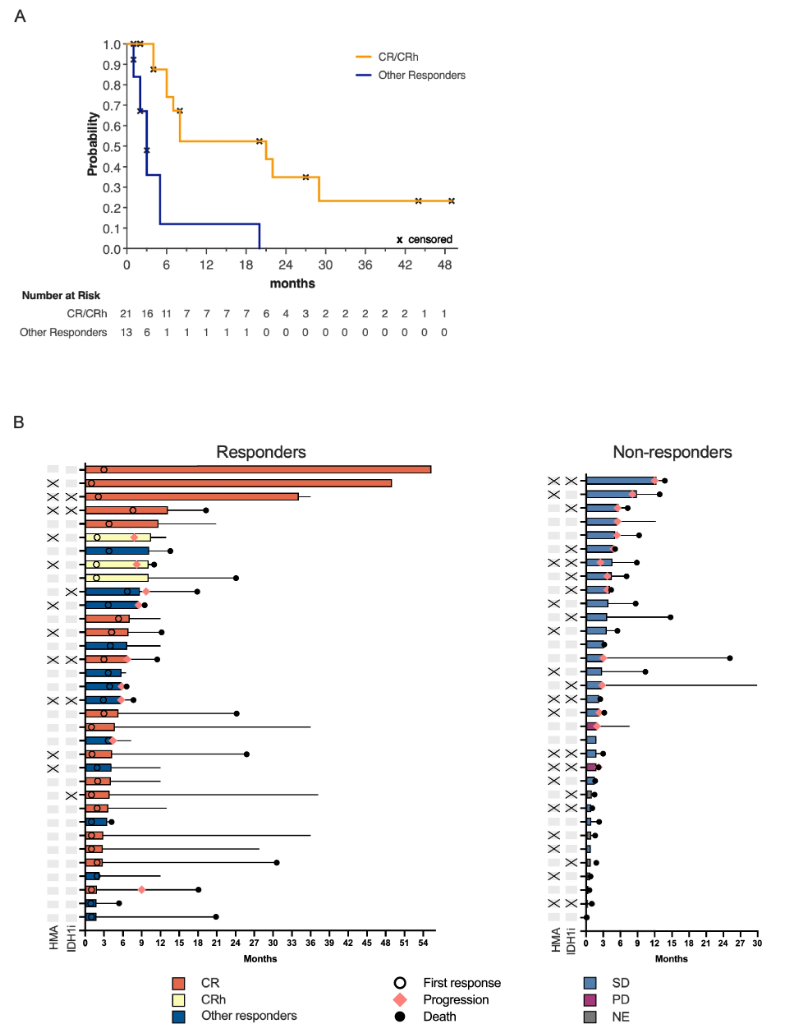
图1:CR/CRh缓解持续时间分析曲线。
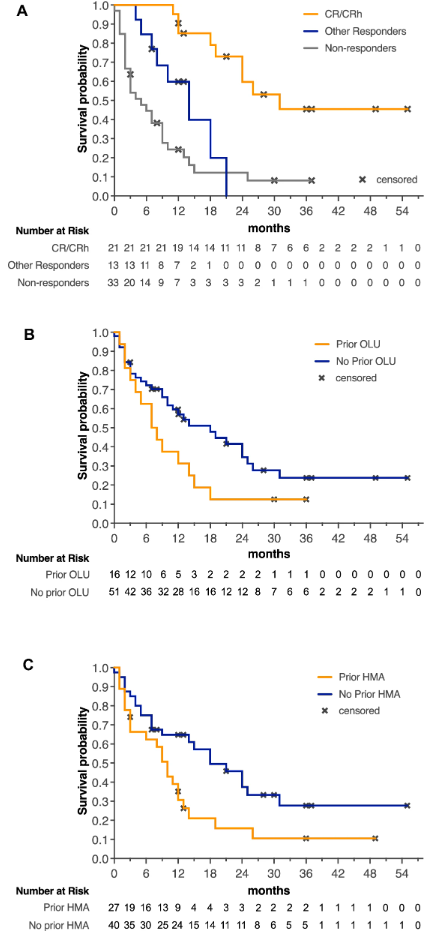
图2:不同患者亚组(既往Olutasidenib或HMA使用)总生存率Kaplan-Meier曲线。
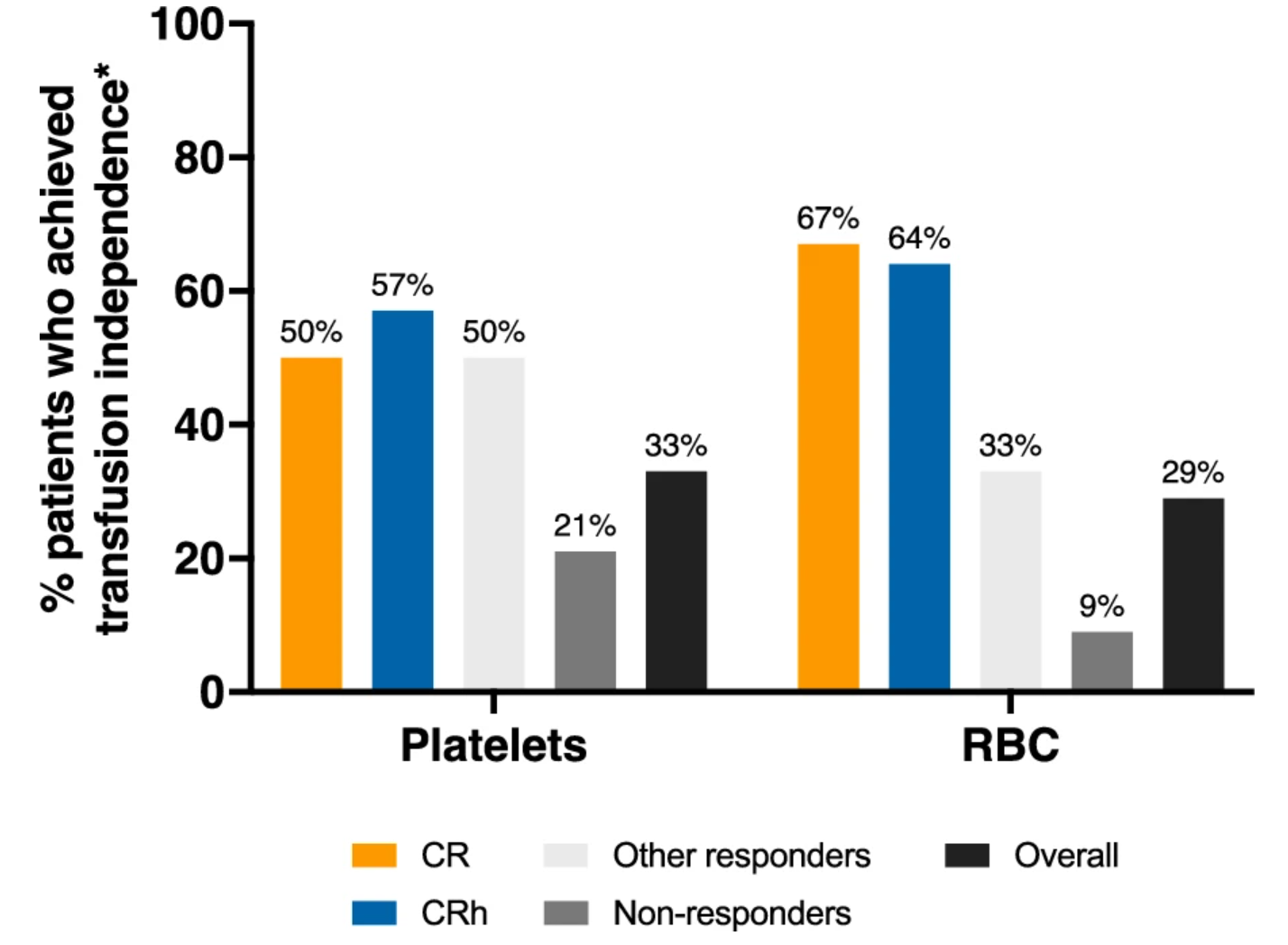
图3:56天输血依赖性缓解率按疗效分组柱状图。
研究价值及意义
本研究首次系统评估了Olutasidenib联合阿扎胞苷治疗复发或难治性mIDH1 AML患者的临床疗效及安全性,显示了显著且持久的缓解与可控的毒副反应谱。相较于已有单药治疗,联合疗法在既往未接受Olutasidenib患者中展现了更高的整体响应率和更长的缓解持续时间,为R/R AML这一高风险患者群体提供了新的治疗选择。
该方案尤其对长期接受HMA或IDH1抑制剂治疗无效的患者同样具有一定疗效,支持以靶向联合化疗策略延缓或克服耐药的发生。此外,显著比例患者成功过渡至HSCT,潜在改善预后。联合治疗整体耐受性良好,毒性未呈叠加趋势,提示安全性可控。
未来研究可围绕以下方向展开:进一步扩大样本量验证疗效,探索与其他靶向药物如Venetoclax的三联组合,及考察该疗法在移植后维持治疗中的作用。深入基因分子特征与反应关系有助于优化患者筛选与个体化治疗。
原始出处
Cortes J E, Roboz G J, Baer M R, et al. Olutasidenib in combination with azacitidine induces durable complete remissions in patients with relapsed or refractory mIDH1 acute myeloid leukemia: a multicohort open-label phase 1/2 trial. Journal of Hematology & Oncology. 2025;18(7). https://doi.org/10.1186/s13045-024-01657-z
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#阿扎胞苷# #急性髓系白血病# #Olutasidenib#
6 举报