JAMA 重磅:Tau PET 阳性率随年龄激增,精准预测阿尔茨海默病认知衰退
2025-06-25 MedSci原创 MedSci原创 发表于上海
该研究强化了Tau PET作为在AD研究和临床实践中生物标志物的定位,有望助力实现早期分层、病理分期及预后判断,为干预时机的选择及疗效监测提供有力工具。
阿尔茨海默病的核心病理包括脑内淀粉样蛋白沉积(Amyloid-β, Aβ)和神经纤维缠结(Tau)。目前,Aβ PET广泛用于早期诊断和临床研究,但其阳性状态在无认知障碍老年人中亦普遍存在,且与未来临床症状的相关性尚不充分。相比之下,神经纤维缠结的分布与临床认知损伤的严重程度高度相关,说明Tau蛋白沉积更贴近症状表现。然而,关于Tau PET阳性在无认知障碍及不同临床阶段的具体频率,以及Tau阳性与认知退化风险的关系,目前文献中仍存在较大争议,尤其是前期研究因定义标准不一导致结果不一致。
近期,发表在顶刊JAMA杂志的一项国际多中心纵向队列研究,汇集全球21个队列共6514名参与者,系统评估了Tau PET阳性在不同认知状态下的发生频率及其相关临床结局风险。该研究采用当下临床认可的Flortaucipir F 18 PET影像视觉判读技术,重点解析Tau神经元纤维缠结与阿尔茨海默病进展的关系,为临床与科研领域提供了更为权威和标准化的证据框架,具有较高临床应用推广价值。

本研究纳入2013年1月至2024年6月期间完成Flortaucipir F 18 Tau PET扫描的6514名参与者,涵盖认知无损、轻度认知障碍、阿尔茨海默病痴呆及其他神经退行性疾病诊断。所有Tau PET扫描均由18名训练合格的专家进行视觉判读,依据已获FDA与EMA批准的标准进行阳性/阴性判定,阳性定义对应于脑神经纤维缠结病理学Braak分期V-VI。大多数参与者同期完成Aβ PET检测。临床随访时间中位数介于1.5至4.0年之间,主要关注事后5年内认知状态恶化(如由无障碍发展至MCI或痴呆)及临床痕迹量表CDR的变化。采用统计学多状态模型及竞争风险调整模型估算临床进展的绝对风险及相关危险比。
研究结果
1. Tau PET阳性频率
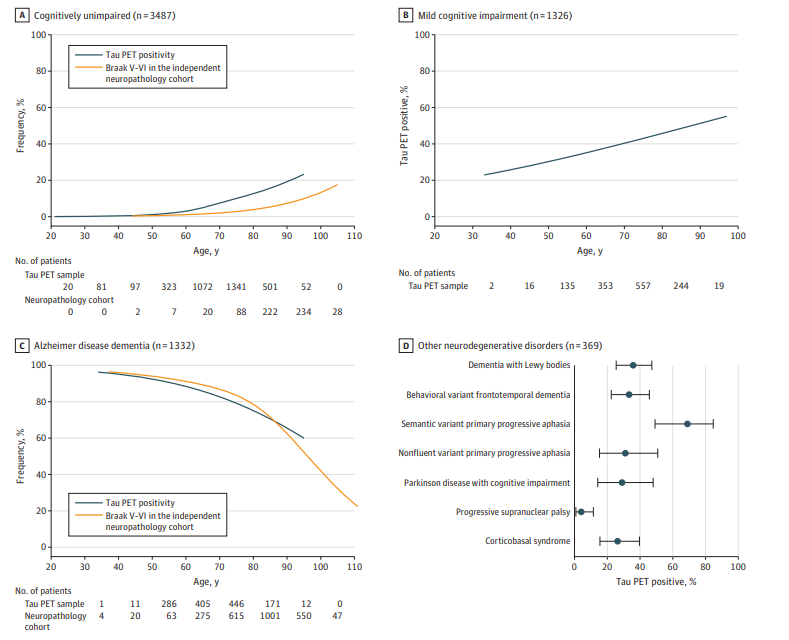
- 认知无损人群(n=3487)中,Tau PET阳性率为9.8%。在50岁以下人群中,阳性率低于1%;60岁时约3%,至90岁增至19%。
- MCI阶段患者(n=1326)Tau阳性率从40岁起即达26%,90岁时升至51%。
- AD痴呆患者(n=1332)Tau阳性比例极高,65岁时达85%以上,随年龄增高呈下降趋势(90岁约65%)。
- 大多数Tau阳性者(92%)同时呈Aβ PET阳性。
图:不同年龄段认知状态群体Tau PET阳性频率曲线
2. Tau PET阳性与阿尔茨海默病临床进展的关联
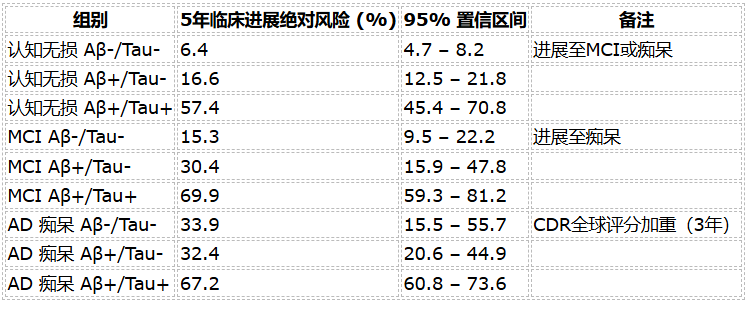
- 认知无损且Aβ+/Tau+个体未来5年发展至MCI或痴呆的绝对风险高达57.4%(95%CI,45.4%-70.8%),远高于Aβ+/Tau-组(17%)及Aβ-/Tau-组(6%)。
- MCI患者中,Aβ+/Tau+组合预示5年内转为痴呆的风险为70%(95%CI,59%-81%)。
- CDR全球评分及量表演变亦反映同样趋势,说明Tau阳性在认知衰退和临床症状恶化中具有强预测价值。
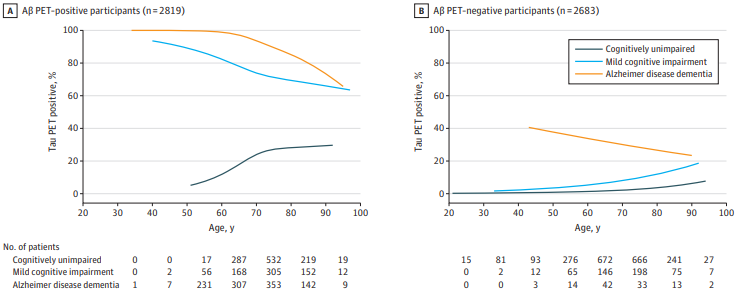
图:Aβ PET阳性与阴性者Tau PET阳性频率对比曲线
3. 其他发现
- Tau PET阳性女性AD患者中频率稍高于男性,APOE ε4携带者更易呈Tau PET阳性。
- 一些非AD神经退行性疾病患者亦观察到Tau PET阳性,尤以部分亚型前额颞叶痴呆为主,临床意义待进一步明确。
结果数据表(关键结果汇总)
研究意义与未来展望
本研究首次在一个庞大且多元国际样本中,应用临床获批标准统一评估Tau PET阳性频率,明确了其在认知无损至AD痴呆全阶段的重要性。结果证明Tau蛋白的PET阳性不仅普遍存在于老龄认知无损者中,且与未来临床认知恶化风险显著相关,特别是在伴随Aβ阳性的情况下。该发现纠正了此前关于Tau阳性率的低估,提示Tau PET检测在AD早期诊断及风险评估中不可或缺。此外,研究提示不同的性别和基因背景(如APOE ε4)可能影响Tau沉积的风险,为精准医学提供潜在指导。
该研究强化了Tau PET作为在AD研究和临床实践中生物标志物的定位,有望助力实现早期分层、病理分期及预后判断,为干预时机的选择及疗效监测提供有力工具。同时,研究亦指出非AD痴呆疾病中异常Tau PET阳性的复杂性,提示未来需探索其机制和临床相关性。这为制订更精准的影像诊断标准和开发针对Tau病理的新型治疗策略提供了依据。
原始出处
Moscoso A, Heeman F, Raghavan S, et al; for the PREVENT-AD Research Group, Harvard Aging Brain Study, LEADS Consortium, and the Alzheimer’s Disease Neuroimaging Initiative. Frequency and Clinical Outcomes Associated With Tau Positron Emission Tomography Positivity. JAMA. Published online June 16, 2025. doi:10.1001/jama.2025.781
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#阿尔茨海默病# #认知衰退# #Tau PET 阳性#
13 举报