CAR-T治疗100例原发或继发CNS淋巴瘤的欧洲真实世界研究
2025-06-13 聊聊血液 聊聊血液 发表于上海
近日《HemaSphere》发表一项基于欧洲血液和骨髓移植学会(EBMT)和GoCART联盟的回顾性研究,进一步补充了CAR-T治疗CNS淋巴瘤的数据。
CAR-T
中枢神经系统(CNS)淋巴瘤分为原发性CNS淋巴瘤(PCNSL)和继发性CNS淋巴瘤(SCNSL),后者指淋巴瘤在疾病过程中扩散至CNS。PCNSL和SCNSL的均预后较差,尤其是在复发或难治性(R/R)情况下。CAR-T细胞疗法在治疗R/R弥漫性大B细胞淋巴瘤(DLBCL)中显示出显著疗效,但CNSL患者通常被排除在CAR-T细胞试验之外,因为担心这些患者发生严重免疫效应细胞相关神经毒性(ICANS)的风险增加。
事实上,多项回顾性研究已经证实CAR-T治疗CNS淋巴瘤安全有效。近日《HemaSphere》发表一项基于欧洲血液和骨髓移植学会(EBMT)和GoCART联盟的回顾性研究,进一步补充了CAR-T治疗CNS淋巴瘤的数据。

研究结果
患者特征:共纳入100名患者,中位年龄62岁,58%的患者接受过≥3线治疗,40%接受过自体干细胞移植。59名患者接受axicabtagene ciloleucel(axi-cel)治疗,38名接受tisagenlecleucel(tisa-cel)治疗。在接受CAR-T时,67名患者存在活动性CNS疾病。
疗效:CAR-T后100天时,CR率为36%、PR率为24%,ORR为60%。24个月时总生存率(OS)和无进展生存率(PFS)分别为37%和28%。24个月时的复发率(RI)为59%,1年非复发死亡率(NRM)为7%。CAR-T时活动性CNS患者的24个月PFS和OS分别为25%和38%;而CAR-T时无CNS受累患者分别为34%和38%。既往接受过移植与改善PFS(35% vs 25%)和OS(47% vs 31%)相关。多因素分析中,LDH>ULN与PFS和RI不佳相关,无因素显著影响OS。
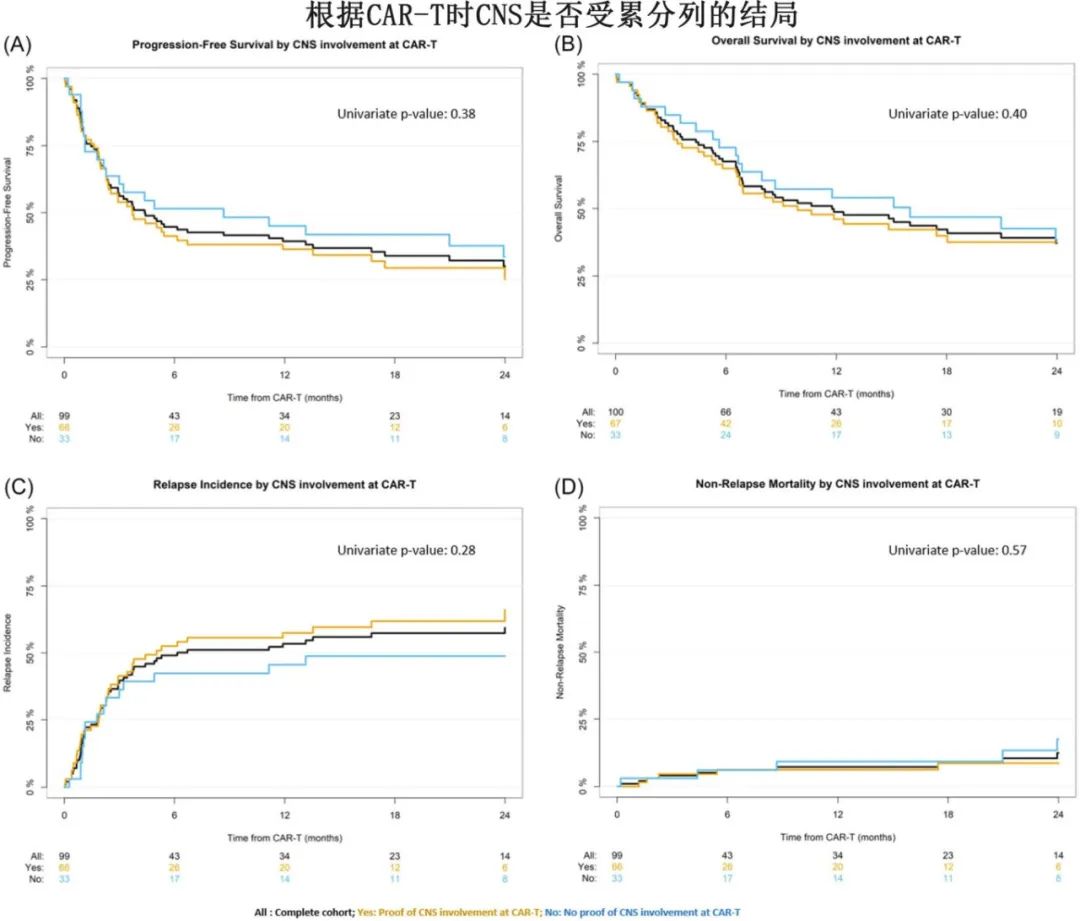
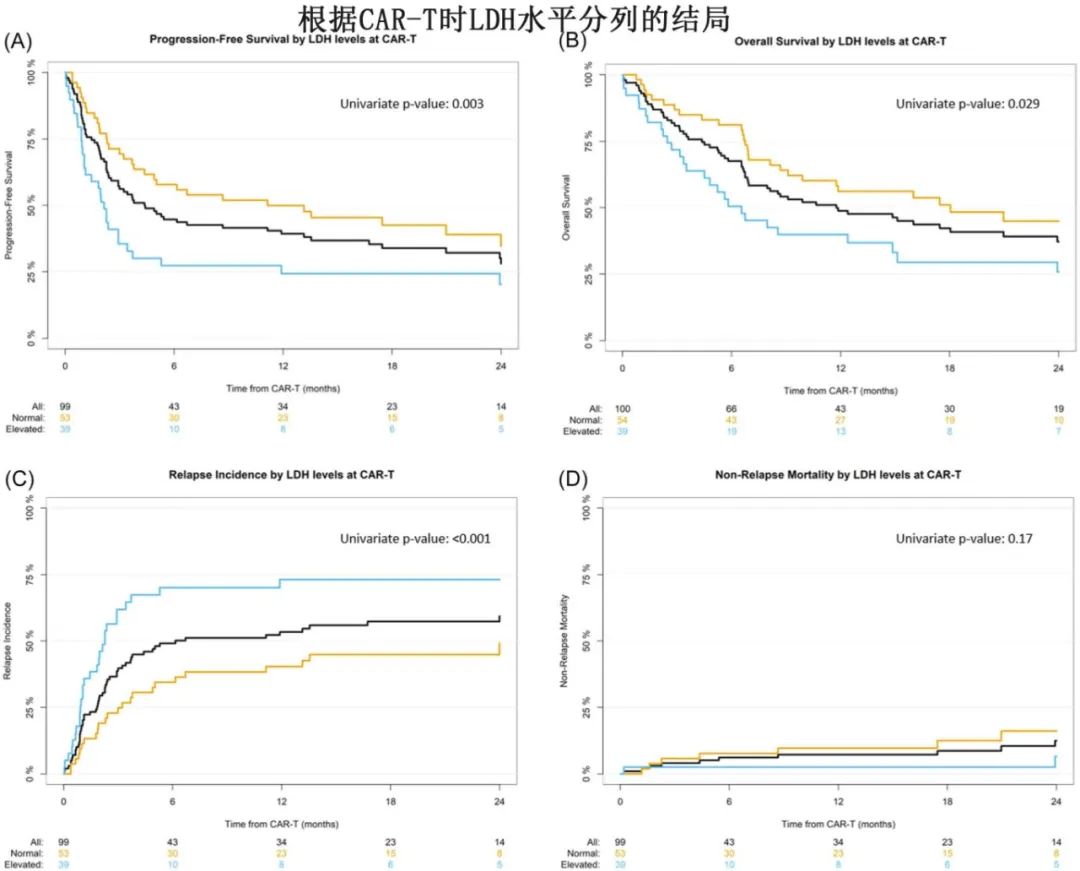
安全性:
CRS和ICANS的发生率分别为83%和42%,其中3级CRS发生率为11%,3-4级ICANS发生率为17%。2名患者因神经毒性死亡,其中1名在CAR-T治疗后第6天死亡,另1名在第133天死于白质脑病。乳酸脱氢酶(LDH)水平升高是RI和PFS的独立风险因素(HR分别为2.4和1.9,p值分别为0.003和0.016)。ECOG评分为2-3的患者发生ICANS的风险显著增加,也是多因素分析中惟一的显著因素(HR 2.68,p=0.002)。83%的患者出现任何级别的中性粒细胞减少,73%出现血小板减少。23%的患者出现3-4级感染,3名患者因感染死亡。
总结
CAR-T在治疗复发或难治性PCNSL和SCNSL患者中显示出一定的疗效和可接受的安全性,包括CRS和ICANS发生率与无CNSL的患者相似,表明CAR-T细胞疗法在CNSL患者中是可行的。尽管CNSL患者通常被排除在CAR-T细胞试验之外,但该研究结果支持将CAR-T细胞疗法作为这些患者的治疗选择。
接受过自体干细胞移植的患者PFS和OS有所改善,而LDH水平升高和ECOG评分较高是不良预后的风险因素,应予以关注。
需要进行更大规模的回顾性分析或前瞻性随机试验,以直接比较CAR-T细胞疗法与自体干细胞移植在CNSL患者中的疗效。进一步研究和创新治疗策略对于改善CAR-T失败后的患者管理至关重要。
参考文献
Ossami Saidy, A., Peczynski, C., Thieblemont, C., Daskalakis, M., Wehrli, M., Beauvais, D., Finke, J., Schorb, E., Vandenberghe, P., Berning, P., Stelljes, M., Ayuk, F., Ram, R., Von Bonin, M., Dreger, P., Bethge, W., Kuhnl, A., Jost, L., Stölzel, F., von Tresckow, B., Renner, C., Fuhrmann, S., Galimard, J.-E., Michel, E., Bazarbachi, A., Balari, A.S., Schmitz, N. and Glass, B. (2025), Efficacy and safety of CAR T-cell therapy in patients with primary or secondary CNS lymphoma: A study on behalf of the EBMT and the GoCART coalition. HemaSphere, 9: e70146. https://doi.org/10.1002/hem3.70146
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言


















#CAR-T# #CNS淋巴瘤#
8