Nat Aging | 大规模血浆蛋白组学研究揭示阿尔茨海默病的诊断生物标志物和相关途径
5小时前 MedSci原创 MedSci原创 发表于上海
本研究通过大规模血浆蛋白组学分析,识别了与AD相关的蛋白,并开发了一个具有临床相关性的预测模型。这些发现不仅揭示了AD的潜在生物学机制,还展示了血浆蛋白作为生物标志物在AD早期检测和治疗决策中的潜力。
阿尔茨海默病(Alzheimer's Disease, AD)是导致痴呆症的主要原因,占所有病例的60%-80%。它主要影响老年人,症状通常在65岁后出现。AD的特征是大脑中淀粉样β斑块的积累、神经纤维缠结和广泛的神经元丢失。近年来,蛋白组学研究揭示了与AD相关的分子途径,并识别了潜在的蛋白生物标志物。这些生物标志物有望用于早期检测、准确诊断和监测疾病进展。然而,以往大多数AD蛋白组学研究集中在大脑或脑脊液(CSF),对血浆蛋白的研究相对较少。血浆蛋白作为生物标志物的潜力尚未被充分挖掘,尤其是在大规模研究中。
近日,国际权威期刊Nature Aging上在线发表了题为“Large-scale plasma proteomic profiling unveils diagnostic biomarkers and pathways for Alzheimer’s disease”的最新研究成果,该研究通过大规模血浆蛋白组学分析,全面检查了超过3300名经过详细表征的个体的6905种寡核苷酸(aptamers),对应6106种独特蛋白,以识别与临床AD状态相关的新蛋白、途径和预测模型。研究识别了416种蛋白(其中294种为新发现),并在两个外部数据集(超过7000个样本)中验证了这些发现。这些与AD相关的蛋白反映了血脑屏障破坏、脂质失调和免疫反应等过程。通过机器学习模型,研究者识别出一组7种蛋白,这些蛋白对临床AD(AUC>0.72)和生物标志物定义的AD状态(AUC>0.88)具有高度预测能力,并在多个外部队列和正交平台上得到了验证。这些发现强调了使用血浆蛋白作为生物标志物的潜力,可用于AD的早期检测、监测以及指导治疗决策。

研究采用三阶段设计:发现、复制和验证。在发现阶段,研究分析了6905种血浆蛋白与临床AD状态的关联,识别出1540种蛋白(1646种寡核苷酸)与AD相关。在复制阶段,416种蛋白(456种寡核苷酸)显示出与AD的显著关联,并在元分析中通过了假发现率(FDR)校正。这些蛋白与AD风险的平均变化相关,平均OR为1.45,最大OR为3.58。
研究进一步在ROS-MAP和GNPC数据集中验证了这些发现。在这些外部数据集中,78%的显著寡核苷酸(353种)显示出一致的效应大小方向,74%(333种)在多重检验校正后仍显著。此外,研究还将结果与六项以往的血浆研究进行了比较,发现37%的蛋白在至少一项以往研究中显著,16%在多重检验校正后显著。
研究还比较了血浆和脑脊液(CSF)中的蛋白组学特征。在456种显著寡核苷酸中,445种在CSF研究中存在,其中174种在CSF中显著。尽管血浆和CSF之间存在一些重叠,但它们的蛋白组学特征似乎不同,表明不同的生物学过程。
研究还探讨了与临床状态相关的蛋白是否能捕捉基于生物标志物的AD病理学。通过CSF淀粉样β和tau状态、淀粉样PET成像和血浆p-tau217状态定义生物标志物状态,研究发现这些蛋白与生物标志物状态之间存在强关联。
研究利用纵向临床数据,识别了与进展为症状性AD相关的蛋白。在456种与临床状态相关的寡核苷酸中,20种也与进展为症状性AD相关。
通过通路分析,研究揭示了与AD相关的蛋白主要涉及五大领域:脂质代谢、免疫和血液学、细胞外基质、神经活动和一般代谢途径。这些途径涉及已知的AD相关蛋白,如APOE、CLU和BIN1,以及新识别的蛋白。
通过多尺度嵌入基因共表达网络分析(MEGENA),研究识别了274个模块,其中M4和M7模块最为显著。这些模块涉及的蛋白在少突胶质细胞、内皮细胞和神经元中富集,强调了细胞外基质和轴突过程在AD中的关键作用。
研究开发了一个基于7种蛋白的预测模型,用于临床诊断或生物标志物状态的预测。该模型在发现测试数据集中的AUC为0.796,在复制数据集中的AUC为0.72。在GNPC队列中,AUC为0.715;在ROS-MAP队列中,AUC为0.757。该模型在预测生物标志物状态时表现更好,AUC超过0.879。
综上所述,本研究通过大规模血浆蛋白组学分析,识别了与AD相关的蛋白,并开发了一个具有临床相关性的预测模型。这些发现不仅揭示了AD的潜在生物学机制,还展示了血浆蛋白作为生物标志物在AD早期检测和治疗决策中的潜力。尽管研究未能建立这些蛋白与AD之间的因果关系,但这些发现为未来的研究提供了重要的方向,尤其是在开发基于血浆的生物标志物方面。研究还强调了进一步验证这些发现的必要性,特别是在独立队列中使用质谱法等正交方法。
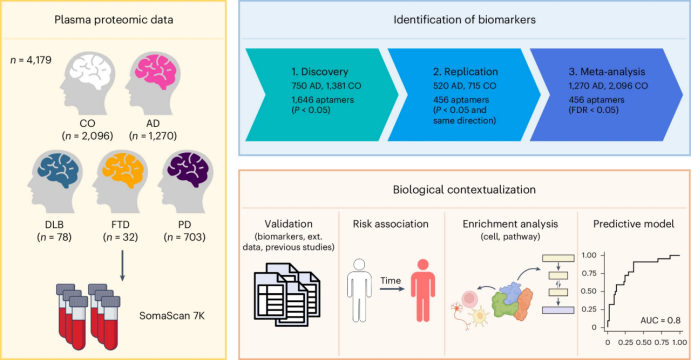
图 本研究模式图
原始出处:
Large-scale plasma proteomic profiling unveils diagnostic biomarkers and pathways for Alzheimer's disease. Nat Aging. 2025 May 20. doi: 10.1038/s43587-025-00872-8. Epub ahead of print. PMID: 40394224.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#阿尔茨海默病# #生物标志物# #血浆蛋白组学#
3