西交大王福/信阳师范许婧ACS Nano:基于双极自供电传感器的机器学习辅助智能监测多变量miRNA生物标志物
2025-03-04 BioMed科技 BioMed科技 发表于陕西省
该研究针对乳腺癌早期诊断中miRNA检测灵敏度低、多靶标同步分析难的问题,开发了一种基于微孔空心立方结构硒化物的双极自供电传感器,实现了对乳腺癌标志物miRNA-451和miRNA-145的高效检测,
乳腺癌作为全球女性恶性肿瘤发病谱系中的首要构成,其发病率呈显著上升趋势,已成为全球公共卫生领域的重大挑战。早期且及时的诊断对于提高乳腺癌患者的生存率至关重要,然而传统检测方法存在诸多局限,使得早期精准诊断困难。
近日,西安交通大学王福团队与信阳师范大学许婧团队在美国化学学会旗下期刊《ACS Nano》发表题为《Machine Learning-Aided Intelligent Monitoring of Multivariate miRNA Biomarkers Using Bipolar Self-powered Sensors》的研究成果。该研究针对乳腺癌早期诊断中miRNA检测灵敏度低、多靶标同步分析难的问题,开发了一种基于微孔空心立方结构硒化物的双极自供电传感器,实现了对乳腺癌标志物miRNA-451和miRNA-145的高效检测,并集成智能终端实现实时动态监测。
MicroRNAs(miRNAs)作为一类内源性非编码RNA小分子,虽然长度仅约18-24个碱基,却在细胞活动中扮演着“基因管理者”的关键角色。它们广泛参与细胞的增殖、发育、分化和凋亡等重要过程。在众多疾病,尤其是癌症中,miRNAs的表达会出现异常,这使得它们成为极具潜力的癌症诊断和治疗靶点。在乳腺癌中,miRNAs通过调控致癌信号通路(如TGF-β、PI3K/AKT)发挥双重作用:miR-145通过靶向TGF-β1抑制癌细胞增殖与迁移,而miR-451的表达下调与化疗耐药性显著相关。因此,同时检测多个miRNAs对于乳腺癌的早期准确诊断意义重大。然而,由于miRNA检测面临序列短(18-24nt)、同源家族相似性高(如let-7家族)、组织表达丰度低(fmol级别)等技术瓶颈,实现其精准检测面临着巨大挑战。
针对上述挑战,本研究团队创新性设计了硒化物微孔空心立方体纳米材料,该材料具备大的比表面积及三维多孔结构,能够显著增加酶的负载量和活性,进而大幅提高检测的灵敏度。基于此,研究团队构建了双极自供电传感器平台,并将其巧妙地集成到商业芯片中。借助智能手机的便捷性,该平台能够实现实时、连续的监测,极大地提升了检测的效率和便捷性。此外,研究团队还引入机器学习技术辅助miRNA检测。通过收集大量实验数据进行模型训练和验证,不断优化算法,有效提高了miRNA检测的准确性和效率,为深入理解miRNA在生物过程中的作用及其与疾病的关联提供了有力支持(图1)。
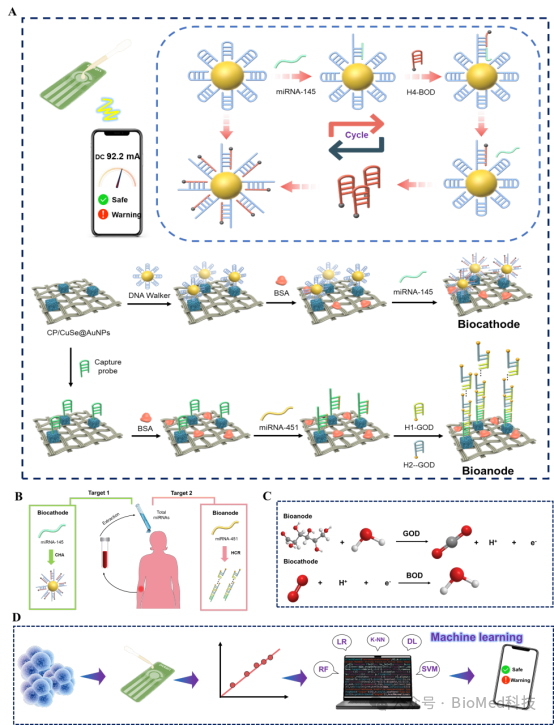
图1. (A) 双极自供电生物传感器miRNA-145和miRNA-451的检测过程。(B) 双目标检测图像。(C) EBFC-SPB工作原理。(D) 机器学习预测miRNA检测结果示意图。
在生物传感界面设计方面,其生物阴极和阳极针对不同的miRNA发挥作用。阴极采用静电吸附固定CuSe/DNA Walker复合探针,在miRNA-145存在时靶向结合并引发催化发夹组装(CHA)循环,生物阳极通过Au-S键共价偶联固定捕获探针,在miRNA-451存在时诱导级联杂交链式反应(HCR)反应,最终由GOD和BOD催化相应反应产生电化学信号。这种双靶点检测设计,有效突破了传统电化学传感器单一检测的局限。
研究团队采用多尺度表征技术对纳米材料进行了系统性分析(图2),通过XRD、Raman、XPS等多种表征手段分析,证实合成的CuSe纳米材料结晶度良好、纯度高,具备出色的导电性,为其作为优质电极基底材料提供了有力的理论依据。SEM和TEM图像表明,CuSe具有规则的形态和良好的分散性,其独特的中空结构有助于提高活性位点利用率和结构稳定性(图3)。
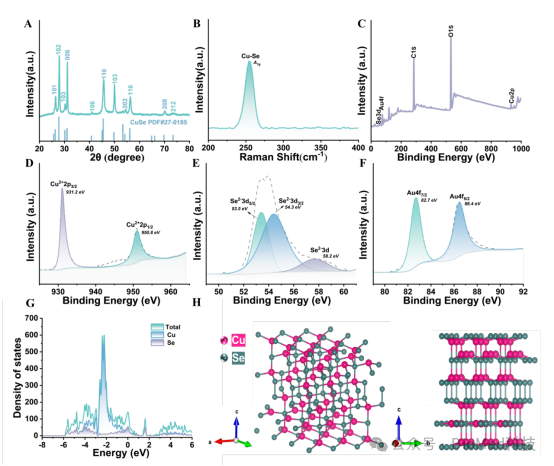
图2. CuSe XRD测量光谱(A)和拉曼光谱(B)。CuSe@AuNPs的XPS全光谱(C)。Cu 2p, Se 3d和Au 4f (D-F)的XPS光谱。CuSe状态密度图(G)。CuSe球棒模型图(H)。

图3. CuSe制备过程(1)和形态特征(2) Cu2O的SEM图像(A)。CuSe的SEM图像(B)。CuSe@AuNPs不同倍率的SEM图像(C-D)。CuSe的TEM图像(E)。CuSe@AuNPs的TEM图像(F-H)。CuSe@AuNPs(1)的EDS映射。
在传感器性能方面,该传感器在1-100000 fM宽线性范围内表现出卓越分析性能。对于miRNA-451和miRNA-145的检测灵敏度分别达到0.240 fM和0.317 fM(S/N=3),瞬时电流响应与目标物浓度呈显著线性相关(R2>0.99)。在实际样品检测中,该传感器的回收率达95.0-105%,相对标准偏差为1.85-4.07%,适用于真实样品检测(图4)。此外,该传感器还具有良好的稳定性、选择性和重复性(图5)。与其他检测方法相比,该双极自供电传感器优势明显,它不仅检测限低、稳定性好,还能在几分钟内完成检测,为实际临床应用提供了极大的便利。
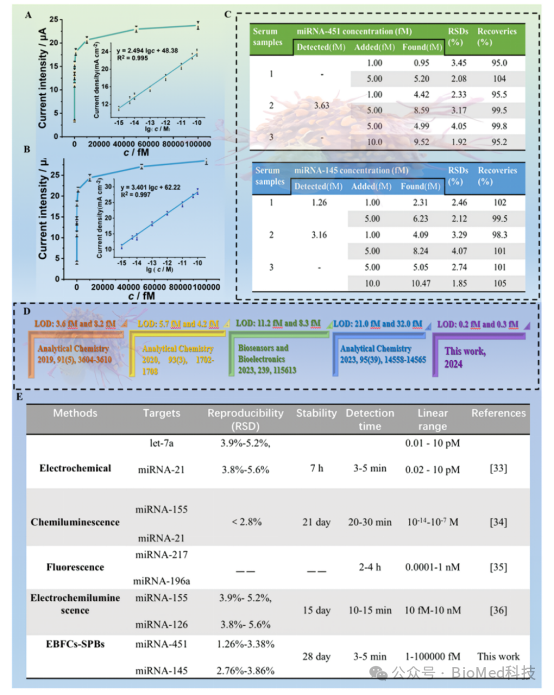
图4. 瞬时电流与miRNA-451浓度的曲线以及瞬时电流与miRNA-451浓度对数在1-100000 fM范围内的线性关系(A)。瞬时电流与miRNA-145浓度函数的曲线以及瞬时电流与miRNA-145浓度对数在1-100000 fM范围内的线性关系(B)。人血清样品(n=3)的分析结果(C)。不同测定方法的比较不同检测方法的分析性能(E)。
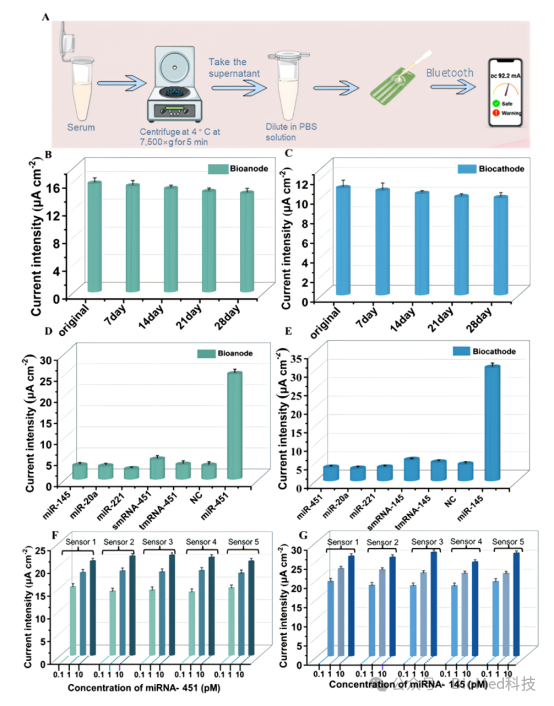
图5. 人血清样品测试过程(A)。构建的生物传感器的稳定性(B-C)。构建的生物传感器的选择性(D-E)。构建的生物传感器的可重复性(F-G)。
机器学习通过数据收集、特征提取、模型训练和验证等一系列步骤,对传感器检测数据进行深度分析,其检测结果显示(图6),基于随机森林(RF)算法建立预测模型,其在性能准确性、召回率等方面表现优异。AUC值高达0.99-1.00。分析不同 miRNA 组合对瞬时电流响应的影响,发现 miRNA-145和miRNA-451联合使用可显著增强响应,模型预测结果与电化学检测结果一致,表明传感器检测灵敏度高。
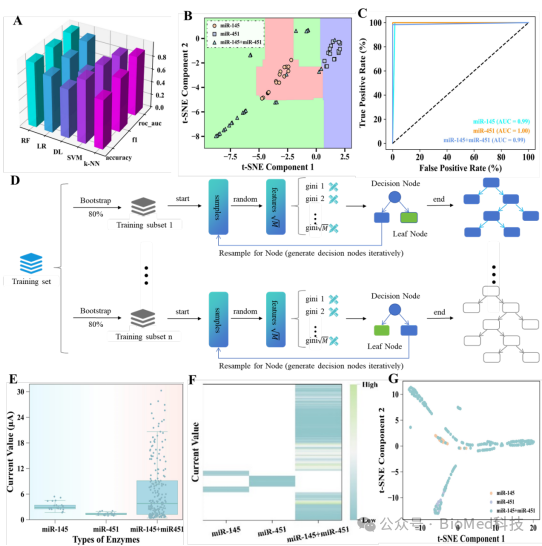
图6. 不同机器学习模型的性能比较(A)。RF模型的决策边界图像(B)。RF模型的ROC曲线(基于五重交叉验证的AUC)(C)。学习模型的基本原理已经开发出来(D)。miRNA实验组之间瞬时电流响应的比较(Tukey HSD检验显示miRNA-145组和miRNA145_451组之间存在显著差异(p = 0.0001)。但miRNA-451组与miRNA-451组间差异无统计学意义(p = 0.843)。miRNA145_451组与miRNA-451组差异显著(p = 0.0008)(E)。全样本瞬时响应电流(F)。t-SNE散点图(G)。
这一科研成果推动了自供电电化学生物传感和生物芯片领域的发展,为新型小型化智能传感器的研发提供了重要思路,更为疾病的早期诊断开辟了新的方向。在未来,随着技术的不断优化和完善,该传感器有望广泛应用于临床实践,实现乳腺癌的早期发现和精准治疗,为全球众多女性的健康保驾护航。
该研究论文第一作者为来自信阳师范大学的许婧副教授,通讯作者是西安交通大学的王福教授。本研究得到了国家自然科学基金、陕西省自然科学基金、河南省高校科技创新团队计划、河南省教育厅项目、信阳师范学院南湖青年学者计划等项目资助。
原文链接:
https://pubs.acs.org/doi/10.1021/acsnano.4c16423
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#乳腺癌# #miRNA#
29