Alzheimer’s Dementia:核苷类逆转录酶抑制剂可显著降低阿尔茨海默病发病风险
18小时前 xiongjy MedSci原创 发表于陕西省
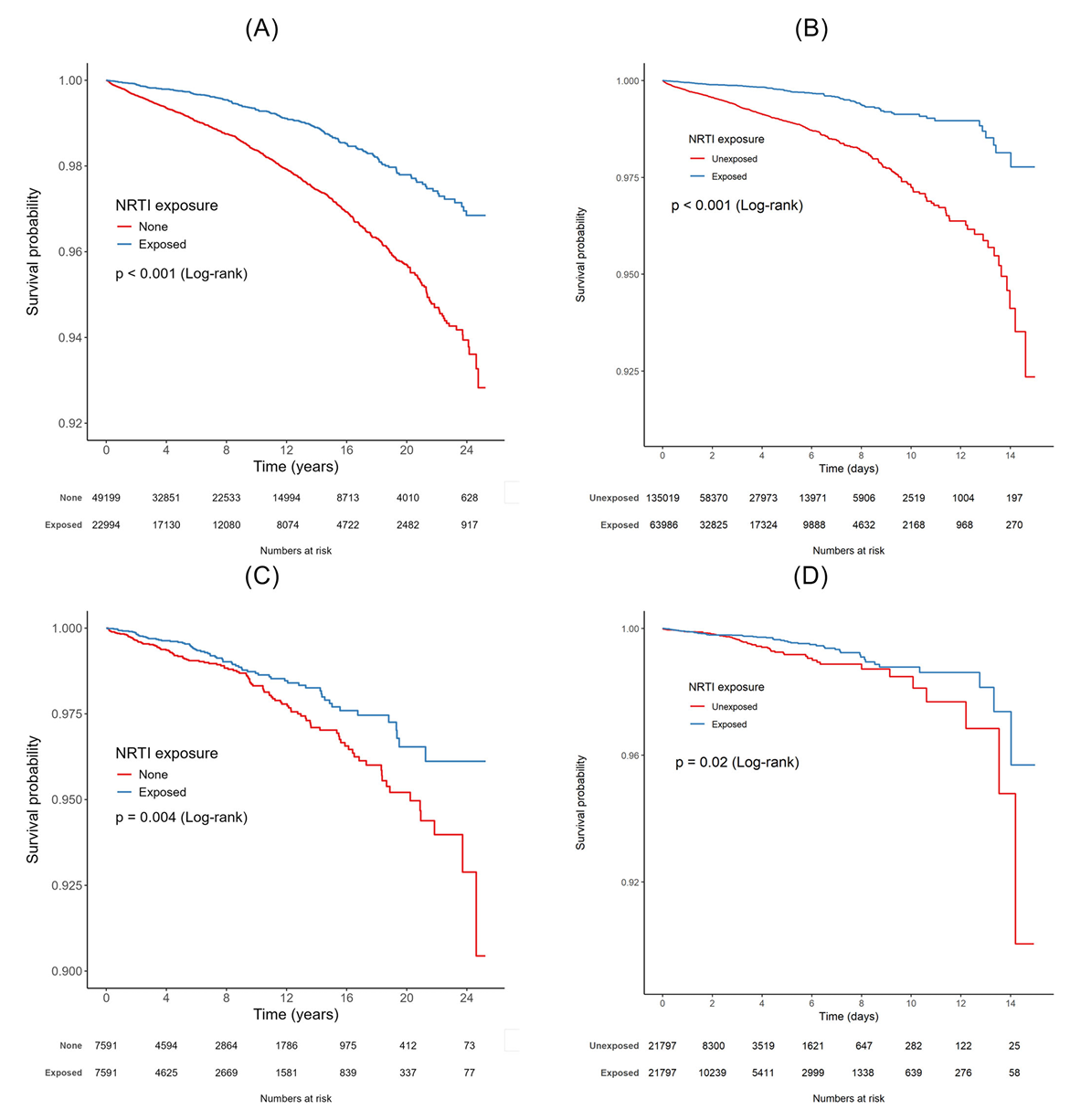
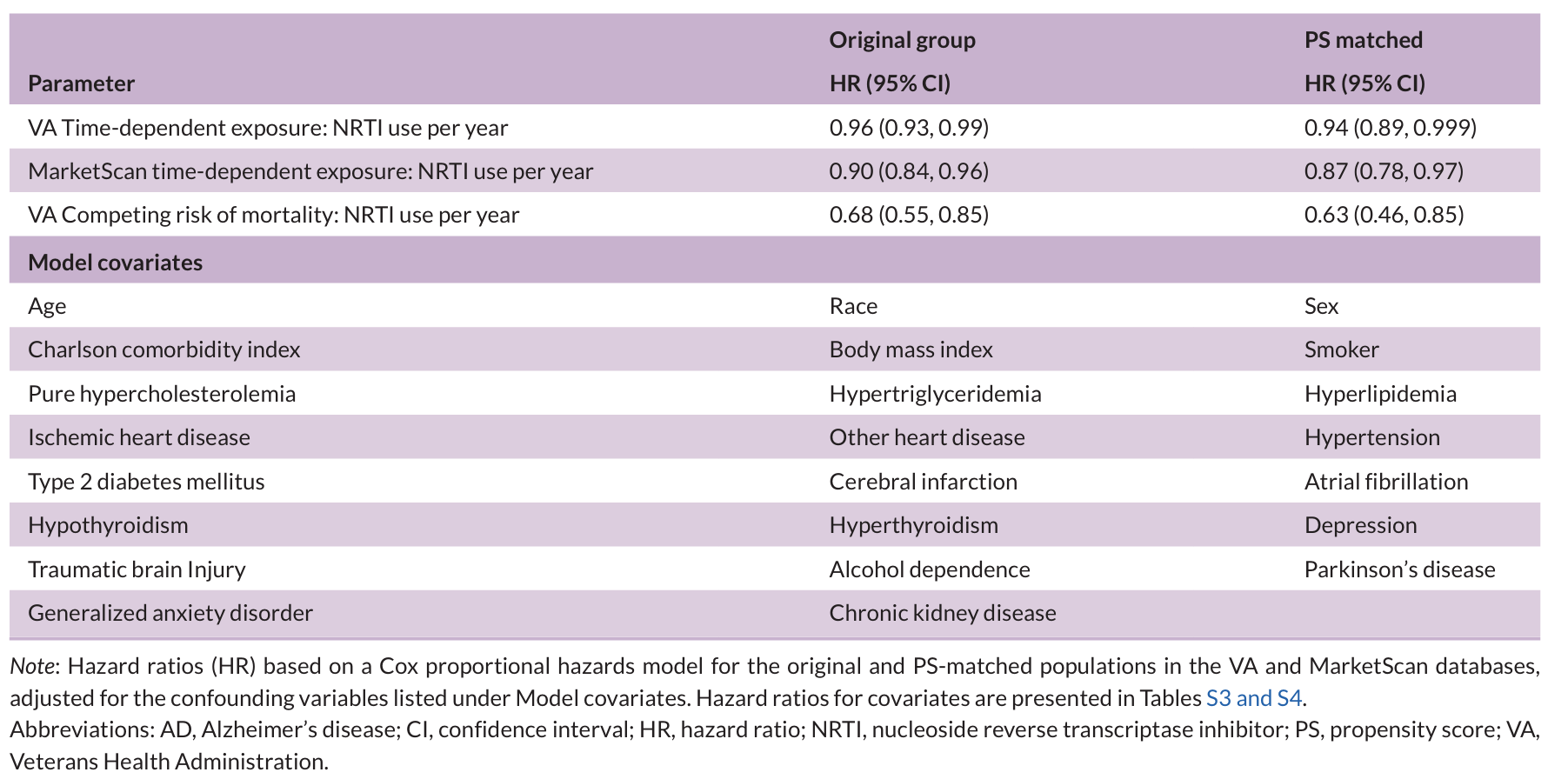
核苷类逆转录酶抑制剂(NRTIs)暴露与阿尔茨海默病风险降低显著相关。VA队列中每年NRTIs使用风险降低4%-6%,MarketScan队列降低10%-13%,且竞争风险模型进一步支持这一关联。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#阿尔茨海默病# #核苷类逆转录酶抑制剂#
2