Chinese Medicine:雷公藤活性成分中线粒体作用的新视角——药效与毒性的双刃剑
2025-07-21 吾乃喵大人 MedSci原创 发表于上海
文章旨在为雷公藤成分临床安全有效利用提供科学依据和创新思路。
研究亮点
- 深入解析中药雷公藤(Tripterygium wilfordii Hook F, TWHF)主要活性成分三萜类化合物对线粒体的双重调节作用,揭示其在发挥药效和引发毒性的关键机制。
- 系统总结线粒体生物生成、融合裂变、线粒体自噬及线粒体介导的凋亡通路在TWHF活性化合物中的作用及其治疗多种肿瘤、代谢和神经疾病的潜力。
- 探讨了雷公藤活性成分的结构优化及纳米药物递送系统设计,围绕线粒体靶向策略提升药效并降低毒性,开启新型临床用药途径。
雷公藤,俗称“雷公藤”,产自中国南方及朝鲜、日本等地,自明代起被应用于多种疾病治疗,如类风湿关节炎等免疫系统疾病。其复杂的化学成分包含多种三萜类、生物碱等活性物质,三氧化二氢龙(triptolide)与雷公藤醇(celastrol)作为代表性成分被证实具备强大的抗炎、抗肿瘤和代谢调节作用,甚至被Cell杂志评为最具药物开发潜力的天然化合物之一。然而,这些天然产物同时引发严重的脏器毒性,极大限制了其临床广泛应用。
当前研究证实,线粒体作为细胞能量代谢和凋亡调控的中心,与雷公藤活性成分的双向调控密切相关。一方面这些药物通过调控线粒体膜电位、ROS水平、融合裂变平衡及自噬通路,促进疾病相关细胞的凋亡或代谢重塑,发挥治疗作用;另一方面,线粒体功能受损又是雷公藤主要毒性的关键机制。因此,深入理解线粒体功能在雷公藤药理学及毒理学中的角色,有助于平衡其疗效与安全,实现更合理的临床应用。
近日,发表在Chinese Medicine杂志上的综述文章系统剖析了TWHF活性化合物对线粒体功能的影响,强调线粒体在介导其药效与毒性中的核心作用。通过汇总大量基础及转化研究数据,文章详细介绍了雷公藤中的主要活性成分:三萜类化合物三氧化二氢龙(triptolide)与雷公藤醇(celastrol)对线粒体生物学及相关信号转导路径的调控,并探讨其在精准剂量设计和纳米递送系统中线粒体靶向的未来应用。文章旨在为雷公藤成分临床安全有效利用提供科学依据和创新思路。

本文为文献综述形式,系统检索并整合近年发表的基础及临床前研究,围绕雷公藤主要活性成分与线粒体多方面相互作用的实验数据和机制解析,重点关注其在肿瘤、代谢障碍、神经退行性疾病及多器官毒性中的表现,兼顾活性分子衍生物、精准药物递送策略以及多药联合治疗的创新探索。
主要研究结果及内容详述
1、雷公藤主要活性成分简介:三氧化二氢龙(Triptolide)与雷公藤醇(Celastrol)
-
雷公藤醇(Celastrol):分子量约450.6 g/mol,1950年代首次从雷公藤提取。其独特结构中的羰基和酚羟基形成内氢键,是其多靶点药理活性的基础。雷公藤醇能够靶向多条信号通路,包括HSP90、NF-κB、PI3K、MAPK通路,调节ROS、炎症反应及细胞凋亡。
-
三氧化二氢龙(Triptolide):1972年分离得到,分子量约360.4 g/mol,结构为环氧萜烯内酯类。三氧化二氢龙通过调控细胞周期、氧化应激和多条信号通路,包括JAK2/NF-κB和Bcl-2家族蛋白,诱导线粒体介导的凋亡,并在多种炎症和肿瘤模型中表现出抑制作用。
此外,诸如三氯雷公藤(Tripchlorolide)和T-96等衍生物也通过类似机制展现相关效应。现代化学结构修饰及纳米递送系统极大提升了这些分子的靶向特异性和生物利用度,进而增强药效、降低毒性。
2、线粒体参与雷公藤药理效应的多条关键通路
雷公藤活性成分主要通过以下机制调节线粒体功能,发挥广泛的抗肿瘤及治疗效应:
-
线粒体凋亡通路激活:调控Bcl-2家族蛋白表达比例、促使细胞色素C(cytochrome c)释放及激活半胱天冬酶级联,诱导肿瘤细胞凋亡。
-
线粒体ROS调节:药物增强或缓解活性氧水平,调控氧化压力,发起细胞命运转变。
-
线粒体融合裂变动态调控:通过蛋白质如Drp1、OPA1维持线粒体形态和数量,影响细胞代谢状态及凋亡敏感性。
-
线粒体自噬(Mitophagy):促进去除受损线粒体,维持细胞稳态,这一过程受到Nur77等转录因子调控。
-
影响线粒体呼吸链复合物活性:如雷公藤醇靶向呼吸链复合物I,调节ATP产量和细胞能量代谢。
这些通路在多种疾病模型中的作用已被实验室和动物研究充分验证(详见下文及表1)。
3、线粒体相关抗肿瘤活性综述
雷公藤中的活性成分作用于多类肿瘤细胞系,通过线粒体介导的途径表现出显著的抗肿瘤活性,具体如下(选摘示例):
| 肿瘤类型 | 活性产物 | 实验模型 | 主要作用靶点及机制 |
|---|---|---|---|
| 非小细胞肺癌(NSCLC) | Celastrol (0.5-4 μM) | A549、H1650等细胞系 | 促使caspase家族激活,Bcl-2下降,Bax上调,线粒体膜电位降低 |
| 肝细胞癌 | Celastrol (2-6 μM) | HepG2等 | 抑制HSP90、EGFR,诱导ROS积累,激活JNK、caspase-3/9通路 |
| 骨肉瘤 | Celastrol/Triptolide | MG-63、U-2OS | 诱导内质网应激,调节Bcl-2家族蛋白,激活caspase家族,引发凋亡 |
| 白血病 | Celastrol/Triptolide | HL-60、U937 | 促ROS生成,激活线粒体凋亡信号,抑制XIAP,释放cytochrome c |
| 乳腺癌 | Celastrol/Triptolide | MCF-7、MDA-MB-231 | 激活线粒体途径,诱导细胞凋亡,调控PI3K/AKT,Ca2+稳态失衡 |
雷公藤活性成分抗肿瘤作用中的线粒体相关靶点与机制
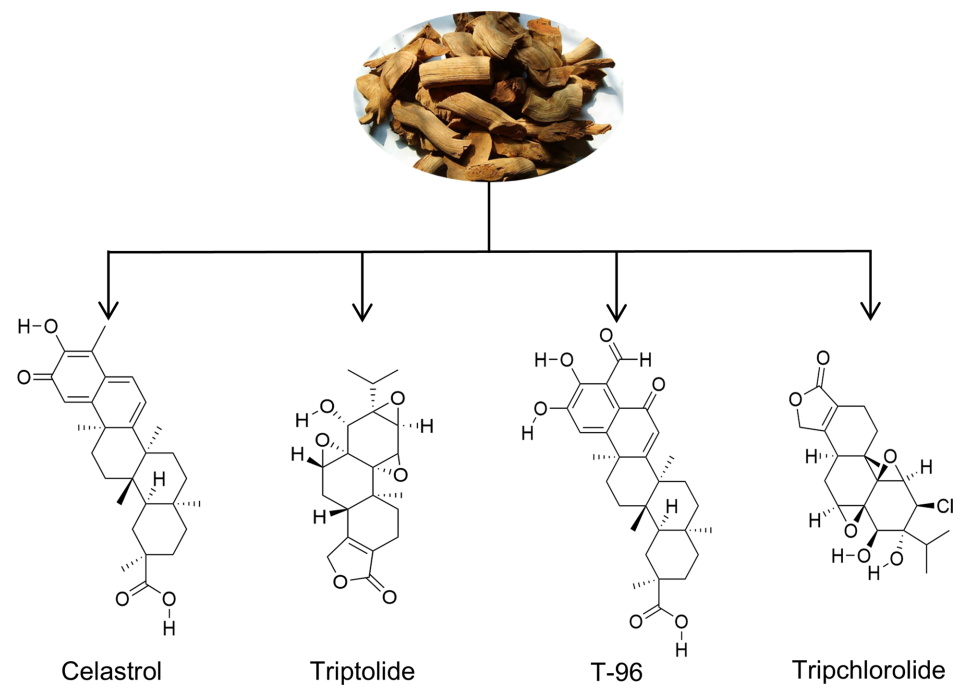
雷公藤主要活性成分的化学结构示意图
4、线粒体在雷公藤代谢疾病和炎症疾病中的作用
线粒体功能障碍已知关联代谢性疾病、胰岛素抵抗及肥胖,雷公藤活性物质通过调节线粒体生物生成、ROS清除及融合裂变动态,逆转细胞代谢异常,从而改善胰岛素敏感性和脂质积累。同时,在炎症疾病如肝炎和急性胰腺炎中,雷公藤醇诱导的Nur77介导线粒体自噬有效清除受损线粒体,缓解炎症反应。
5、线粒体介导的雷公藤毒性机制
雷公藤活性成分尤其是三氧化二氢龙,造成多器官毒性,主要包括:
-
肝毒性:通过干扰线粒体呼吸链,导致NADH/NAD+失衡及过量ROS产生,激活Drp1介导的线粒体裂变、自噬及凋亡,导致肝细胞死亡。
-
生殖毒性:三氧化二氢龙破坏能量代谢和线粒体动力学,降低精子活力与卵母细胞品质。
-
心脏毒性:通过抑制Nrf2,增加氧化应激,介导p53依赖的线粒体凋亡途径。
-
肾毒性:诱导线粒体功能失调,激活ROS介导的PANoptosis程序性细胞死亡,触发免疫信号通路、肾功能损伤。
-
耳毒性:干扰内耳干细胞线粒体融合蛋白OPA1功能,抑制线粒体融合。
三氧化二氢龙通过线粒体介导的毒性机制总结
| 毒性类型 | 实验模型 | 主要发现与机制 |
|---|---|---|
| 肝毒性 | 大鼠、细胞系 | 抑制线粒体呼吸链,Drp1介导线粒体裂变及凋亡 |
| 抗肝肾毒性综合 | 小鼠 | 诱导PANoptosis,促ROS及线粒体DNA损伤,cGAS-STING通路活化 |
| 生殖毒性 | 小鼠、大鼠 | 干扰能量代谢,异常线粒体形态及膜电位,ROS/JNK信号通路激活 |
| 心脏毒性 | 小鼠、心肌细胞 | 抑制Nrf2导致氧化应激,p53依赖性线粒体凋亡 |
| 耳毒性 | 内耳干细胞 | 剪切OPA1,抑制线粒体融合 |
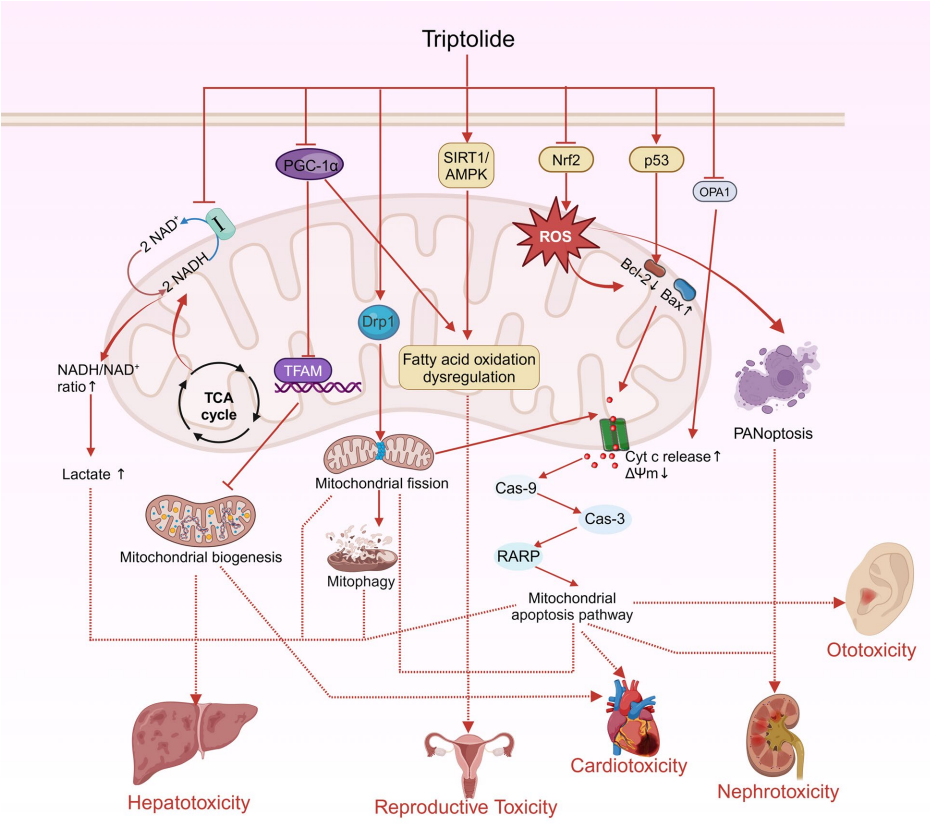
三氧化二氢龙诱导毒性中的线粒体功能障碍途径示意图
3.6 雷公藤活性成分的线粒体靶向优化及纳米递送系统
针对雷公藤活性物质生物利用度低、毒性大的短板,研究者通过分子结构修饰(如三苯基膦TPP修饰)和纳米载体设计(微乳、聚合物胶束、脂质体等)实现高效线粒体靶向递送,显著提升药物治疗索引。相关代表性递送系统及其特点总结如下:
| 药物 | 递送平台 | 粒径 | 载药效率(EE%) | 载药负载(LE%) | 应用模型 | 组成与功能 | 主要优点及疗效 |
|---|---|---|---|---|---|---|---|
| Celastrol | 微乳 | ~40nm | 94.5% | 41.0% | HeLa细胞三维肿瘤球 | 转铁蛋白修饰,提高肿瘤靶向性的微乳 | 增强抗宫颈癌疗效,促凋亡 |
| Celastrol | 聚合物胶束 | 60-120nm | 71-92% | 12-15% | MCF-7, A549细胞系及裸鼠 | 三苯基膦修饰、多重靶向微环境响应释放 | 提高肿瘤线粒体特异性释放,抑制能量代谢,增强抗肿瘤作用 |
| Celastrol | 脂质体 | 89nm | 98.4% | - | HepG2及裸鼠 | 表面透明质酸包被,实现肿瘤及线粒体双重靶向 | 提升肿瘤靶向摄取及细胞凋亡 |
| Triptolide | 脂质体 | 133nm | 62.7% | 0.76% | 胰腺癌模型 | 三苯基膦修饰脂质体,靶向线粒体 | 增强胰腺癌抗肿瘤效果,降低系统毒性 |
| Triptolide | 纳米水凝胶 | 81nm | 83.5% | 4.52% | 乳腺癌细胞及小鼠 | 热敏性释放,增强线粒体介导凋亡 | 持续药物释放,协同抑制肿瘤血管生成和肿瘤生长 |
雷公藤活性成分线粒体靶向纳米递送系统汇总
此外,创新联用策略,如与其他中药复方、抗氧化剂或线粒体保护剂共用,有效缓解三氧化二氢龙的多器官毒性,为转化临床应用提供有力支持。
研究价值与未来展望
本文系统梳理了雷公藤及其代表活性成分三氧化二氢龙与雷公藤醇通过线粒体通路发挥多重生物学效应的最新进展,突出展示了线粒体作为治疗和毒性关键介质的双重作用特性。通过细致揭示其在凋亡、ROS调控、线粒体动力学与自噬中的复杂相互关系,本文为电子化学改造与精确纳米靶向递送提供理论指导和技术方向。尤其是在癌症、代谢疾病及神经疾病等领域,基于线粒体机制的精准用药策略有望破解高效治疗与低毒风险的临床难题。
同时,文章指出了当前对雷公藤线粒体作用机制认知尚存不足,提示未来需要:
- 深入解析雷公藤活性成分在不同细胞类型及微环境中对线粒体多维网络的调节差异。
- 探索更多活性衍生物及其联合用药在减毒增效中的作用。
- 开发更精准的多级靶点递送体系,实现高病灶选择性和最低系统副作用。
这些努力将为雷公藤相关天然产物临床转化奠定坚实基础。
原始出处
Liu ZH, Li D, Yang XW, Chen XS, Fu CX. The emerging role of mitochondria in the pharmacological and toxicological effects of Tripterygium wilfordii Hook F: functions, targets and new therapeutic applications. Chinese Medicine. 2025;20:114. https://doi.org/10.1186/s13020-025-01170-6
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#病毒性# #雷公藤# #药效#
6 举报