JCO | EXCLAIM-2试验:莫博替尼一线治疗EGFR外显子20插入突变阳性NSCLC的III期研究
2025-02-11 daikun MedSci原创 发表于陕西省
该研究比较了莫博替尼与铂类化疗作为一线治疗EGFR ex20ins阳性晚期/转移性NSCLC患者的疗效和安全性,结果显示,莫博替尼的疗效并不优于铂类化疗,未达到研究终点。
表皮生长因子受体(EGFR)外显子20插入(ex20ins)突变约占所有EGFR突变阳性非小细胞肺癌(NSCLC)病例的6%-12%。第一代和第二代EGFR酪氨酸激酶抑制剂(TKI)在EGFR ex20ins阳性NSCLC患者中的客观缓解率(ORR)约为10%,无进展生存期(PFS)约为1-3个月。铂类化疗通常作为EGFR ex20ins突变患者的首选一线治疗,其ORR为24.6%-47.0%,中位PFS为5.6-7.1个月,中位总生存期(OS)为19.6-24.4个月。然而,基于真实世界证据,铂类化疗的中位PFS范围为4.2-6.4个月,突显了EGFR ex20ins阳性NSCLC患者对有效治疗的需求。

方法
EXCLAIM-2是一项全球性的III期、开放标签、多中心、随机、活性对照研究,比较了莫博替尼(mobocertinib)与铂类化疗作为一线治疗EGFR ex20ins阳性晚期/转移性NSCLC患者的疗效和安全性。入组患者为既往未接受治疗的EGFR ex20ins阳性局部晚期或转移性NSCLC患者,随机分配(1:1比例)接受莫博替尼 160 mg每日一次口服,或研究者选择的静脉化疗(培美曲塞+顺铂或培美曲塞+卡铂)。化疗组患者在接受四周期化疗(每3周一次)后接受培美曲塞维持治疗。化疗组患者在接受BICR评估的疾病进展后,如果符合条件,可以交叉到莫博替尼治疗。主要终点是BICR评估的无进展生存期(PFS)。关键次要终点包括BICR评估的确认的ORR和OS。其他次要终点包括研究者评估的PFS和确认的ORR、BICR和研究者在评估的DoR、TTR和DCR、患者报告症状的TTD、以及使用EORTC QLQ-C30和EORTC QLQ-LC13评估的健康相关生活质量(HRQoL)。安全性终点是治疗引起的不良事件(TEAEs)。
研究结果
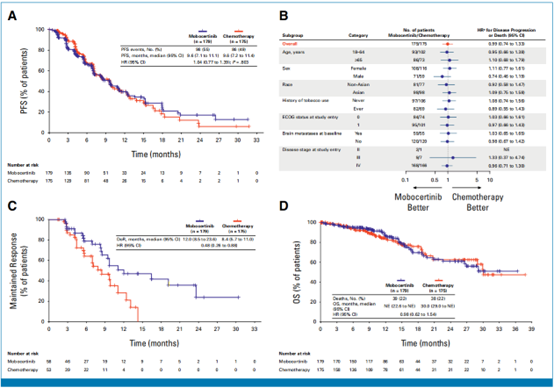
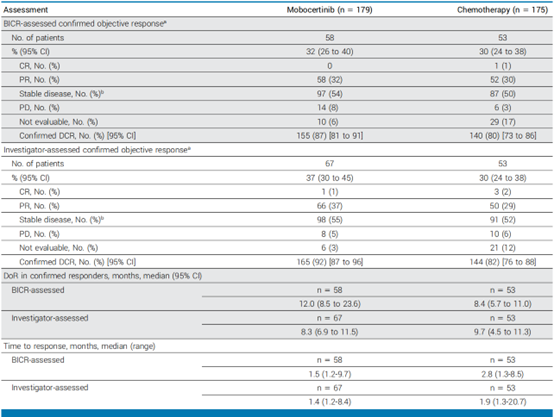
共有354例患者被随机分配(莫博替尼组:n=179;化疗组:n=175)。基线特征在两组之间均衡。在期中分析(IA)(截止日期:2023年4月4日)时,BICR评估的中位PFS在两组中均为9.6个月(风险比[HR],1.04 [95% CI,0.77至1.39];P = .803)。主要终点超过了预设的无效边界(HR > 1)。BICR评估的确认的ORR(95% CI)在莫博替尼组为32%(26至40)与化疗组为30%(24至38);中位DoR为12.0个月与8.4个月。生活质量评估表明,与化疗组相比,莫博替尼组肺癌症状、认知功能和便秘恶化的时间明显延迟。
安全性分析
莫博替尼组>5%的患者出现的3级以上不良事件(AE)包括腹泻(20%,1%)、贫血(6%,10%)、脂酶升高(6%,0%)和白细胞减少(1%,7%)。
结论
EXCLAIM-2试验未达到其主要终点。对于一线治疗EGFR ex20ins阳性晚期/转移性NSCLC患者,莫博替尼的疗效并不优于铂类化疗。
原始出处
Jänne PA, Wang B, Cho BC, et al. First-Line Mobocertinib Versus Platinum-Based Chemotherapy in Patients With EGFR Exon 20 Insertion–Positive Metastatic Non–Small Cell Lung Cancer in the Phase III EXCLAIM-2 Trial. J Clin Oncol. 2025;JCO2101269. https://doi.org/10.1200/JCO.21.01269
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#NSCLC# #III期研究# #铂类化疗# #莫博替尼#
24
表皮生长因子受体(EGFR)外显子20插入(ex20ins)突变约占所有EGFR突变阳性非小细胞肺癌(NSCLC)病例的6%-12%。
15