Adv Sci:福建医科大学陈实等人研究发现cCCT2可作为PDAC化疗敏感性标志物,其通过抑制DDR促进肿瘤细胞衰老
昨天 iNature iNature 发表于上海
该研究整合临床样本、单细胞转录组测序、蛋白质组学和 RNA 测序,揭示 FOLFIRINOX(5-氟尿嘧啶、奥沙利铂、伊立替康和亚叶酸钙的联合方案)治疗可诱导更高比例的衰老肿瘤细胞 (senTC)。
联合化疗和免疫疗法在胰腺导管腺癌 (PDAC) 治疗中未能取得突破。化疗诱导衰老是解决这一问题的潜在方案。
2025年7月21日,福建医科大学陈实、Li Qiaowei、Wang Zuwei共同通讯在Advanced Science 在线发表题为“SenExo-cCCT2 Reprograms Senescence Response and Anti-Tumor Immunity Following FOLFIRINOX Chemotherapy in Pancreatic Ductal Adenocarcinoma”的研究论文。该研究整合临床样本、单细胞转录组测序、蛋白质组学和 RNA 测序,揭示 FOLFIRINOX(5-氟尿嘧啶、奥沙利铂、伊立替康和亚叶酸钙的联合方案)治疗可诱导更高比例的衰老肿瘤细胞 (senTC)。
这一现象主要归因于 cCCT2 的存在,它通过调控小泛素样修饰物偶联抑制 SLX4 凝聚物介导的 DNA 损伤修复途径,从而促进肿瘤细胞衰老。在肿瘤免疫微环境中,cCCT2过表达的senTC表现出衰老相关分泌表型(SASP),优先分泌CXCL10,从而诱导CD8+ T细胞趋化。基于cCCT2的促衰老和免疫微环境重塑作用,该研究开发了一种工程化的外泌体负载环状RNA系统SenExo-cCCT2。FOLFIRINOX方案与SenExo-cCCT2联合使用可增强胰腺癌细胞诱导衰老的能力。随后,抗PD-L1疗法可促进免疫介导的senTC清除,显著提高胰腺癌化疗联合免疫治疗的疗效。

胰腺导管腺癌(PDAC)恶性程度极高,化疗是进展期PDAC的一线治疗方案。目前,该病的主要治疗方案包括FOLFIRINOX方案(5-氟尿嘧啶、奥沙利铂、伊立替康和亚叶酸钙的联合方案)和AG方案(吉西他滨联合白蛋白结合型紫杉醇)。虽然FOLFIRINOX方案在临床治疗中疗效优于AG方案,但耐药性仍然是PDAC面临的一大挑战。因此,阐明化疗耐药的分子机制并寻找增强化疗敏感性的策略至关重要。一些研究团队尝试通过化疗和免疫疗法相结合来提高胰腺癌细胞对化疗的敏感性,但其临床疗效有限。这些局限性与胰腺癌(PDAC)免疫微环境的异质性有关,包括肿瘤细胞中不同程度的CD8+ T细胞浸润和程序性死亡配体1 (PD-L1) 的差异性表达。PD-L1表达仍然是PDAC患者免疫疗法敏感性的重要标志,但在这些患者中往往表达不足。因此,迫切需要发现决定治疗反应的其他机制。
目前化疗相关的研究主要集中于药物诱导的细胞凋亡,却忽略了治疗诱导的细胞衰老的关键作用。作者观察到,与AG方案相比,FOLFIRINOX方案在胰腺癌细胞中诱导了更明显的衰老表型,并且衰老程度与化疗反应和预后呈正相关。衰老肿瘤细胞 (senTC) 促进肿瘤微环境中衰老相关分泌表型 (SASP) 的形成,从而募集 CD8+ T 细胞从外周循环渗入肿瘤环境。然而,衰老是一把双刃剑。尽管化疗诱导的肿瘤细胞衰老最初是化疗敏感性的指标,但在肿瘤微环境重塑过程中,持续存在的 senTC 可以在结束休眠后逃脱生长停滞,从而导致干细胞特性增强和耐药性增强。此外,senTC 往往表现出免疫检查点共抑制分子 PD-L1 表达增加,从而逃避免疫介导的清除。抗 PD-L1 疗法与衰老免疫清除策略相结合,似乎是一种可行且具有潜在协同作用的提高化疗敏感性的策略。
增强化疗后senTC的诱导是规避治疗局限性的潜在策略。目前促进衰老的方法主要依赖于扩增核DNA损伤以触发不可逆的细胞周期停滞,而化疗药物是主要手段。DNA损伤修复(DDR)的内在能力仍然是化疗耐药性的关键决定因素。FOLFIRINOX是一种由四种药物组成的强效化疗方案,可诱导多种类型的DNA损伤,包括DNA-蛋白质交联(DPC)、链间交联(ICL)和双链断裂(DSB)。因此,FOLFIRINOX方案增加了衰老细胞的负担。然而,尽管最初接受FOLFIRINOX治疗的患者表现出更高的敏感性,但由于免疫抑制的肿瘤微环境,他们随后可能会产生耐药性和复发。 SLX4 作为修复复合物中的支架蛋白,调控相分离驱动的生物分子凝聚物,而这些凝聚体在各种形式的 DDR 中发挥着至关重要的作用。因此,SLX4 可能介导 FOLFIRINOX 诱导的肿瘤细胞衰老。阐明控制 SLX4 凝聚体形成的分子机制有望增强细胞对 FOLFIRINOX 的化学敏感性。
越来越多的证据表明环状 RNA (circRNA) 是 DDR 通路的调控因子。先前的研究表明,circRNA 不仅介导化学耐药性,还调节细胞衰老和免疫细胞浸润。因此,研究假设 circRNA 通过调控 DDR 通路来驱动衰老和免疫微环境重塑,从而增强化学敏感性。在该研究鉴定出一种与衰老相关的环状RNA cCCT2,它在化疗反应性胰腺导管腺癌 (PDAC) 患者中上调。cCCT2通过抑制SLX4的小泛素样修饰物结合(SUMO化)来增强肿瘤细胞衰老。通过体外和体内模型,该研究证明cCCT2通过衰老增强作用增强化疗增敏并促进免疫浸润。因此,作者设计了一个基于生物相容性外泌体的递送平台SenExo-cCCT2,以实现高效的环状RNA治疗有效载荷递送。SenExo-cCCT2联合FOLFIRINOX化疗诱导的衰老以及抗PD-L1抗体序贯治疗,可有效清除senTC,从而增强PDAC化疗的疗效。
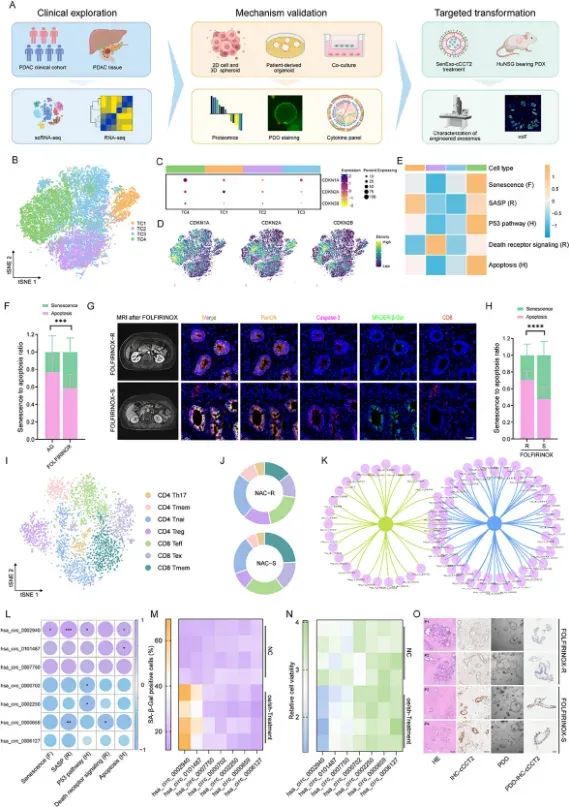
图1 PDAC中肿瘤细胞衰老与化学敏感性及CD8+ T细胞浸润的相关性(图源自Advanced Science)
参考消息:
https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202508431
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言


















#胰腺导管腺癌# #肿瘤细胞衰老#
11 举报