Nature Medicine:阿里联手浙肿发布全球首个胃癌影像筛查AI模型,平扫CT+AI实现大规模胃癌早筛
2025-06-26 梅斯肿瘤新前沿 MedSci原创 发表于上海
浙江省肿瘤医院与阿里达摩院研发的胃癌影像筛查 AI 模型 DAMO GRAPE 登《Nature Medicine》,用平扫 CT 识别早期胃癌,提升检出率,具卫生经济学优势。
今日,浙江省肿瘤医院联合阿里巴巴达摩院发布的全球首个胃癌影像筛查AI模型DAMO GRAPE,不仅登上国际顶级期刊《Nature Medicine》,更以颠覆性的技术路径,为破解胃癌早筛困局提供了全新解法。这项成果,首次利用平扫CT影像识别早期胃癌病灶,并联合全国20家医院,在近10万人的大规模临床研究中大幅提升胃癌检出率。

从“不可能”到“可能”:AI如何突破胃癌筛查技术天花板
据国家癌症中心统计,我国每年新发胃癌约36万例,死亡26万例,死亡人数在所有恶性肿瘤中位列第三。如能在早期发现并干预,患者的5年生存率可从30%以下显著提升至90%以上。
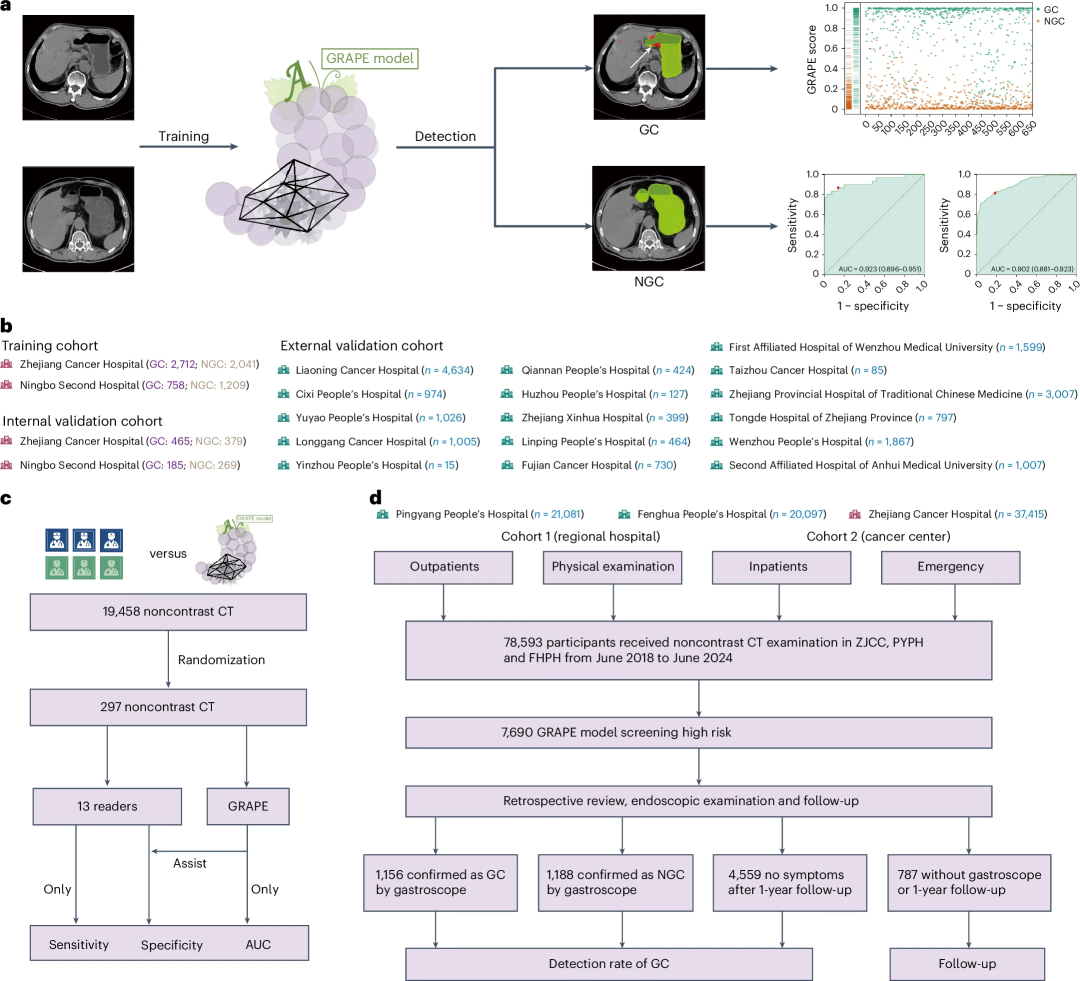
图示:GRAPE 的开发、评估和临床转化概述
传统医学认知中,平扫CT并非胃癌筛查的理想工具。胃部特殊的解剖结构——充盈状态差异大、内容物干扰多、早期病灶常局限于黏膜层,使得CT影像对微小病变的检出率长期受限。
基于此,研发团队构建了国际最大规模的胃癌平扫CT影像多中心数据集,覆盖全国20个医学中心近10万例样本。通过深度学习算法,模型成功捕捉到人眼难以察觉的影像特征:胃壁厚度0.2毫米的异常增厚、黏膜表面0.1毫米的纹理改变、胃小区形态的微妙变异。这些突破性进展,让平扫CT首次具备识别早期胃癌的能力。
在模拟机会性筛查试验中,该模型展现出惊人的临床价值。对常规腹部CT检查人群进行回顾性分析时,AI成功提前2-10个月发现胃癌病灶。
DAMO GRAPE的敏感性和特异性分别达到85.1%和96.8%,相比放射科医生分别提升21.8%和14.0%。这令平扫CT识别早期胃癌首次成为可能,也让“平扫CT+AI”在多癌筛查上更进一步。
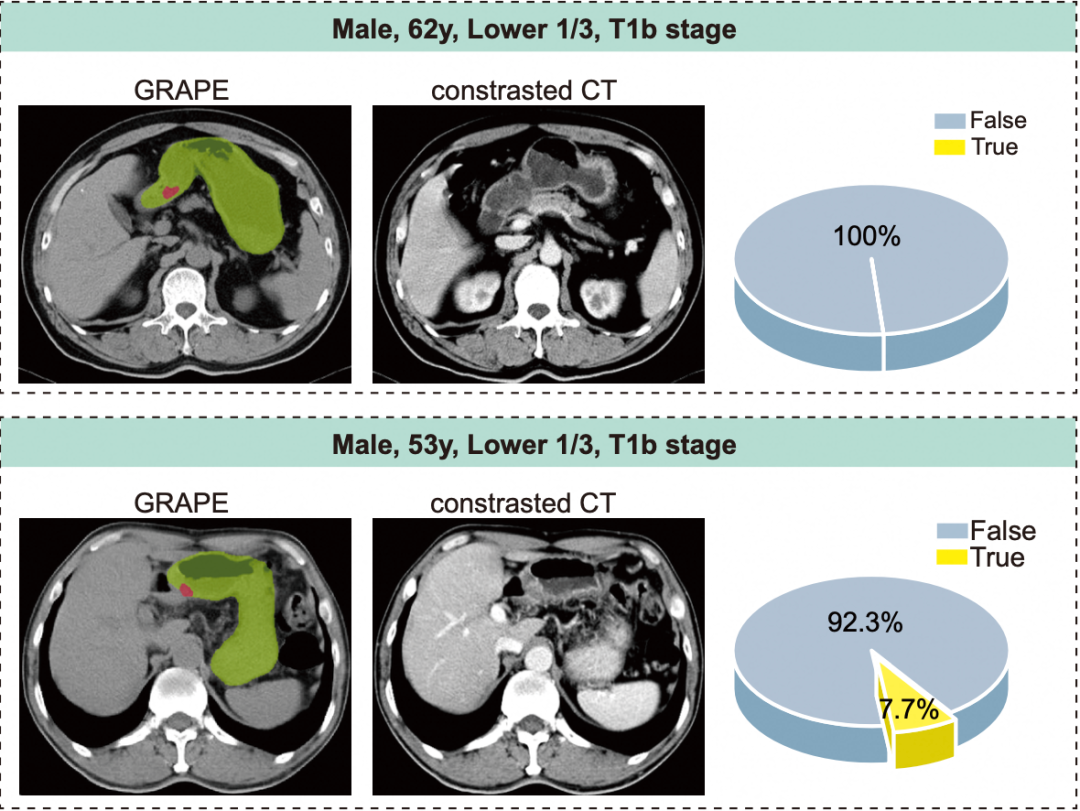
AI成功从平扫CT种识别早期胃癌
从实验室到诊室:AI模型重塑胃癌防治路径
这项技术突破带来的不仅是诊断能力的跃迁,更是筛查范式的革新。传统“问卷筛查+胃镜”模式面临两大痛点:胃镜依从率不足30%,基层医院内镜诊断水平参差不齐。DAMO GRAPE模型提出的“平扫CT+AI”两步法,为破解困局提供了新路径。
在浙江某地区医院的试点中,AI初筛使胃癌检出率提升至24.5%,较传统模式提高24.5倍。更值得关注的是,检出病例中近40%为无症状早期患者,这类人群正是降低胃癌死亡率的关键突破口。模型敏感性达85.1%、特异性达96.8%的优异表现,意味着每100例AI提示阳性的病例中,约85例最终确诊胃癌,同时有效避免假阳性带来的过度医疗。
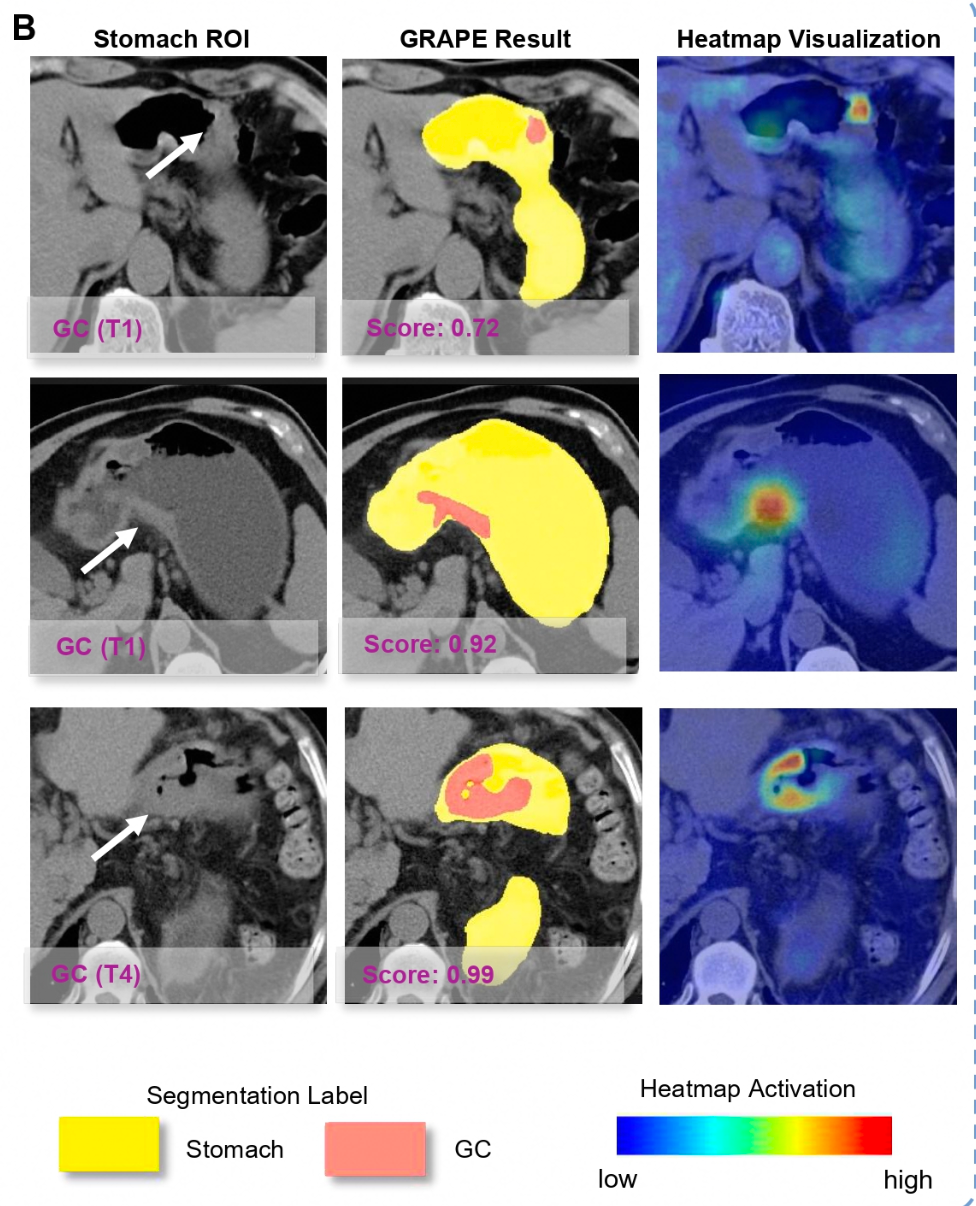
AI能识别各阶段胃癌
例如,其中1名45岁患者因腹部不适接受胃镜检查,确诊局部晚期胃癌,而该患者6个月前因其他疾病做过胸腹部平扫CT检查,当时未报告腹部病变。胡灿将这张旧片子导入AI模型,提示存在胃癌病灶。也就是说,如果6个月前就有AI自动筛查,这名患者将有机会更早确诊并接受治疗。
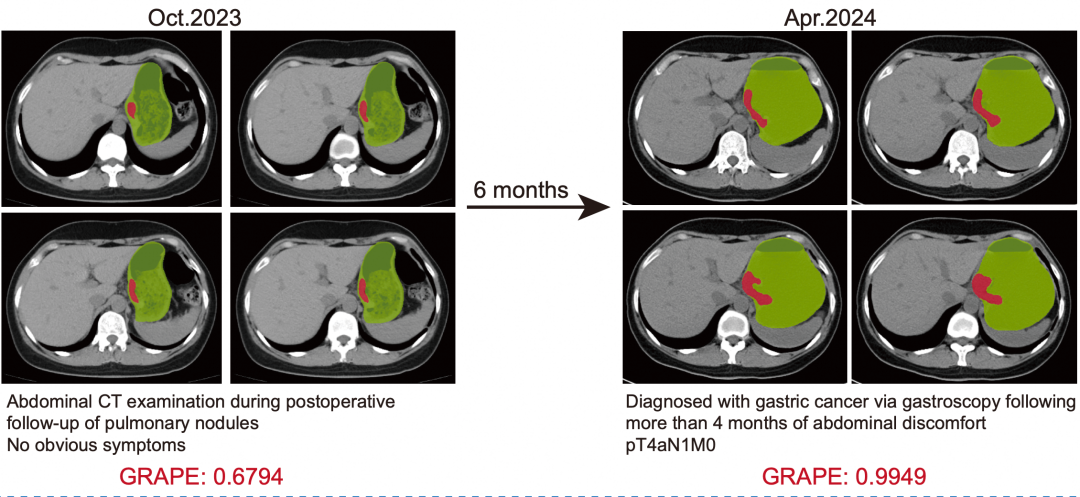
AI提前6个月识别出胃癌
从卫生经济学视角审视,该模型展现出显著优势。平扫CT作为常规体检项目,检查成本仅为增强CT的1/3,且无需注射造影剂。当AI分析嵌入现有CT工作流程时,相当于在现有医疗资源基础上,免费获得胃癌筛查功能。这种“一石二鸟”的创新模式,为医疗资源薄弱地区提供了可行方案。
结语
研发团队并未止步于胃癌突破。基于相同技术框架,阿里达摩院已开发出覆盖胰腺癌、结直肠癌、肝癌等5大癌种的筛查模型,构建起“平扫CT+AI”的多癌种早筛体系。在浙江、安徽等地,该技术已嵌入区域肿瘤防治网络,实现“检查即筛查”的被动式防控。
更深远的影响在于诊疗模式的变革。当AI成为影像科医生的“第二双眼睛”,临床决策链条被重塑:AI完成海量影像数据的初筛,医生聚焦疑难病例的精准诊断。这种人机协同模式,既保留医生的临床决策权,又通过技术赋能提升整体诊疗水平。正如程向东教授所言:“AI的价值不在于替代医生,而在于让医生更早发现那些‘看不见’的病灶。”
参考来源:
1.https://www.nature.com/articles/s41591-025-03785-6
2.阿里巴巴
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#胃癌# #AI模型#
18 举报