论文解读|黄启钊/许力凡/陈志宇教授揭示头颈鳞癌中Treg细胞应答调控新机制
2025-05-29 Genes and Diseases Genes and Diseases 发表于上海
该研究揭示了Bcl6通过组蛋白H3K4三甲基化维持HNSCC中Treg细胞的谱系稳定性与抑制功能,为缓解HNSCC免疫抑制性微环境,增效免疫治疗提供新的潜在干预靶点。
头颈部恶性肿瘤主要发生于口腔、咽部和喉部等部位,其中90%以上为头颈部鳞状细胞癌(Head and neck squamous cell carcinoma, HNSCC)。近年来,HNSCC发病率快速上升且总体预后较差。尽管采用手术、放疗和化疗等综合治疗手段,超过65%的局部晚期HNSCC患者仍会出现复发或转移,而晚期或复发性HNSCC尚无有效治疗手段。目前,免疫检查点阻断(Immune checkpoint blockade therapy,ICB)疗法在多种癌症中展现出显著疗效。帕博利珠单抗(Pembrolizumab)是首个获批用于治疗转移性或复发性HNSCC的ICB抗体。然而,仅少数HNSCC患者能从ICB治疗中获益,这主要归因于免疫抑制性肿瘤微环境(Tumor microenvironment, TME)。调节性T(Regulatory T cells, Treg)细胞是TME中免疫抑制细胞的主要亚型,其与抗肿瘤免疫反应受损及免疫逃逸密切相关。研究表明,瘤内Treg细胞数量增加及Treg/CD8+T细胞比值升高与HNSCC患者不良临床结局相关。然而,HNSCC发生过程中调控Treg细胞的潜在机制仍不明确。
重庆医科大学免疫创新与转化研究院黄启钊教授团队联合陆军军医大学全军免疫学研究所许力凡教授及西南医院陈志宇教授团队在本刊发表了题为“Bcl6 controls the stability and suppressive function of regulatory T cells in head and neck squamous cell carcinoma”的研究论文。该研究揭示了Bcl6通过组蛋白H3K4三甲基化维持HNSCC中Treg细胞的谱系稳定性与抑制功能,为缓解HNSCC免疫抑制性微环境,增效免疫治疗提供新的潜在干预靶点。
01 Treg 细胞缺失Bcl6显著减缓头颈鳞癌进展
研究人员利用4NQO 诱癌模型发现,KO(Treg细胞特异性缺失Bcl6)小鼠较对照(WT)小鼠病损数量少、体积小;KO小鼠病损大多呈颗粒状、斑块状,而 WT 小鼠有更多病损呈现为疣状、菜花状。
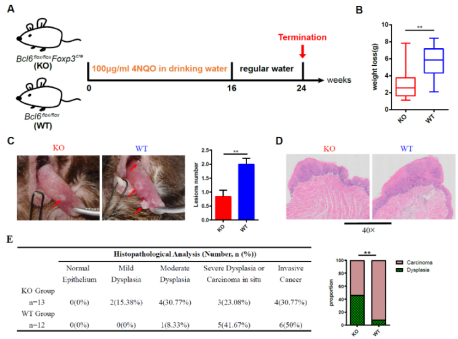
图1 Treg 细胞缺失Bcl6显著减缓头颈鳞癌进展 (原文中Figure1)
02 Treg 细胞缺失Bcl6增强TME和肿瘤引流淋巴结内T细胞免疫应答
引流淋巴结(Draining lymph node, dLN)是肿瘤抗原特异性 CD8+T细胞启动和活化的首要部位,通过流式细胞术分析,研究人员发现,KO小鼠dLN幼稚CD8+T细胞比例显著低于WT小鼠,而中央记忆CD8+T细胞及效应记忆CD8+T细胞比例显著高于WT小鼠。相应的,KO小鼠肿瘤浸润T细胞比例显著高于WT小鼠。KO小鼠肿瘤浸润和引流淋巴结CD8+T细胞细胞因子分泌均显著高于WT小鼠。
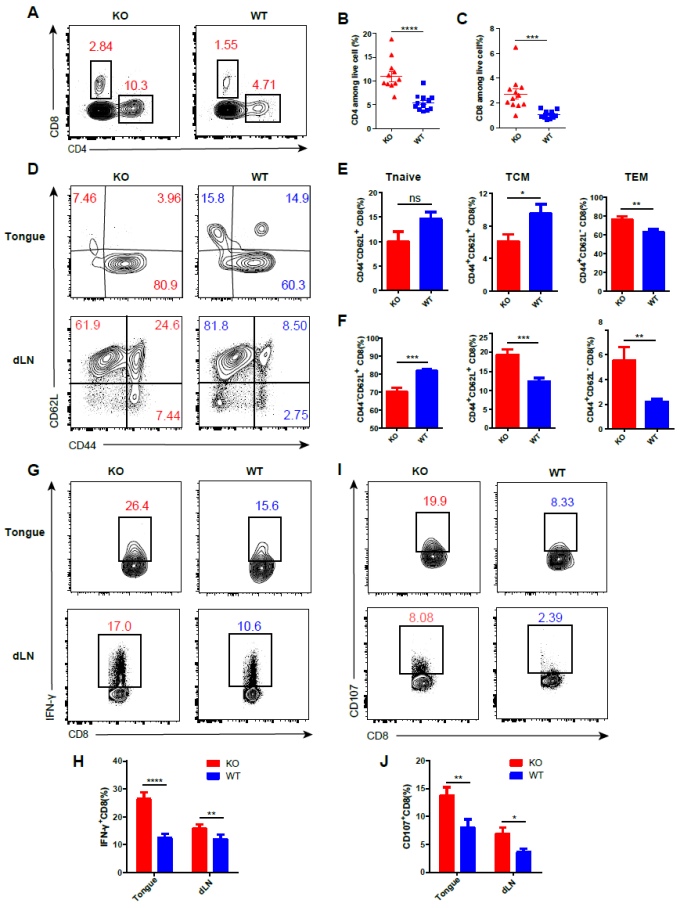
图2 Treg 细胞缺失Bcl6增强TME和dLN内T细胞免疫应答(原文中Figure 2)
03 Treg 细胞缺失Bcl6损害了Treg细胞的抑制功能RF8通过
研究团队进一步分析发现,尽管Treg细胞比例无显著差异,但Bcl6敲除导致TME及dLN中Treg细胞的Foxp3表达水平显著下调,提示Bcl6对维持Treg细胞谱系稳定性具有关键作用。体外抑制实验显示,与WT Treg细胞相比, KO 组Treg细胞的免疫抑制能力明显减弱。Treg细胞中Bcl6的缺失导致dLN中效应性Treg细胞减少,从而为CD8+T细胞的充分活化提供有利环境,促使具有更强效应功能的CD8+T细胞向舌部浸润增加。
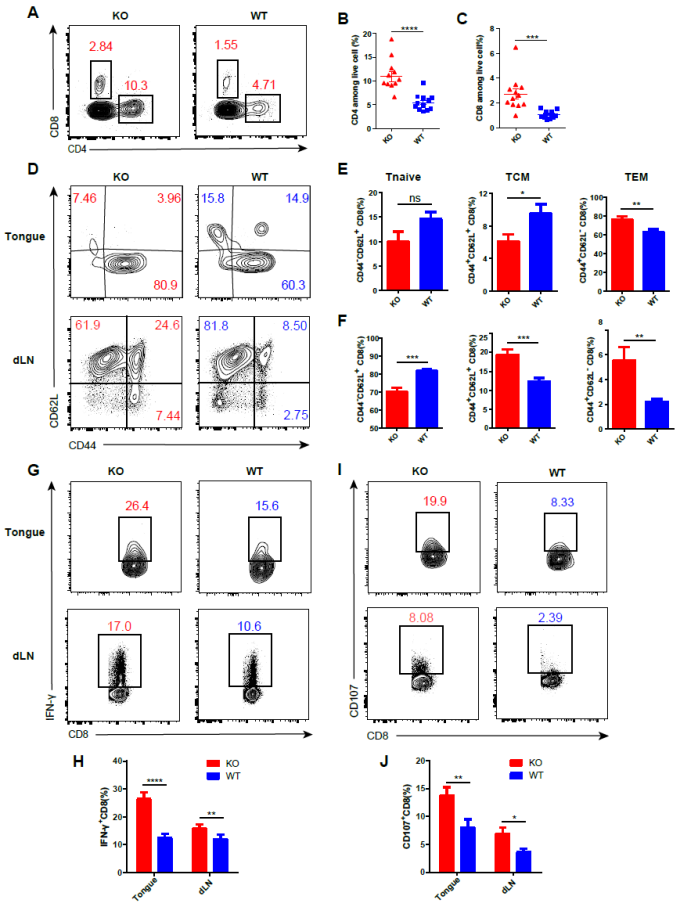
图2 Treg 细胞缺失Bcl6增强TME和dLN内T细胞免疫应答(原文中Figure 2)
04 Bcl6可能通过组蛋白H3K4三甲基化维持Treg细胞的谱系稳定性
为揭示Bcl6调控HNSCC中Treg细胞的作用机制,研究团队进行了RNA测序(RNA-seq)。基因本体(Gene ontology, GO)通路分析表明,与WT Treg细胞相比,KO Treg细胞中下调基因显著富集于与基因激活相关的组蛋白H3K4甲基化通路。RT-qPCR结果进一步显示,KO Treg细胞中H3K4转甲基酶基因(包括Kmt2a、Kmt2c和Kmt2d)表达显著降低。既往研究表明,Kmt2d可通过重塑增强子表观景观促进Treg细胞发育。流式细胞术检测发现,与WT Treg细胞相比,KO Treg细胞中组蛋白H3K4三甲基化水平(而非单甲基化)显著降低。
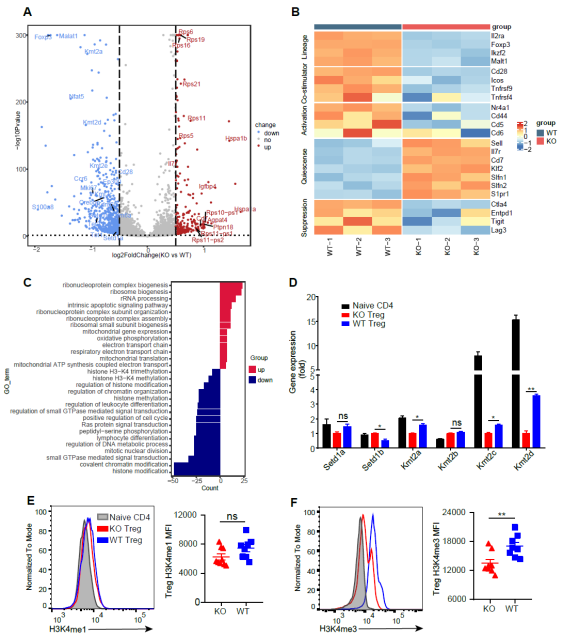
图3 Bcl6可能通过组蛋白H3K4三甲基化维持Treg细胞的谱系稳定性(原文中Figure4)
05 Bcl6抑制剂FX1增强ICB抗体对HNSCC的疗效
FX1 是第一个报道的对 Bcl6 BTB 结构域的亲和力高于内源性辅助抑制蛋白的抑制剂,研究团队发现使用FX1可显著抑制小鼠HNSCC肿瘤生长,并进一步增强ICB疗法的治疗效果。与KO小鼠实验结果一致,FX1处理降低了dLN中Treg细胞的Foxp3、CD25、GITR和ICOS表达水平。值得注意的是,FX1单药治疗组及联合治疗组的dLN和肿瘤浸润淋巴细胞中Treg/CD44+CD8+T细胞比值均显著降低,表明FX1的治疗效果主要通过调控Treg细胞介导。
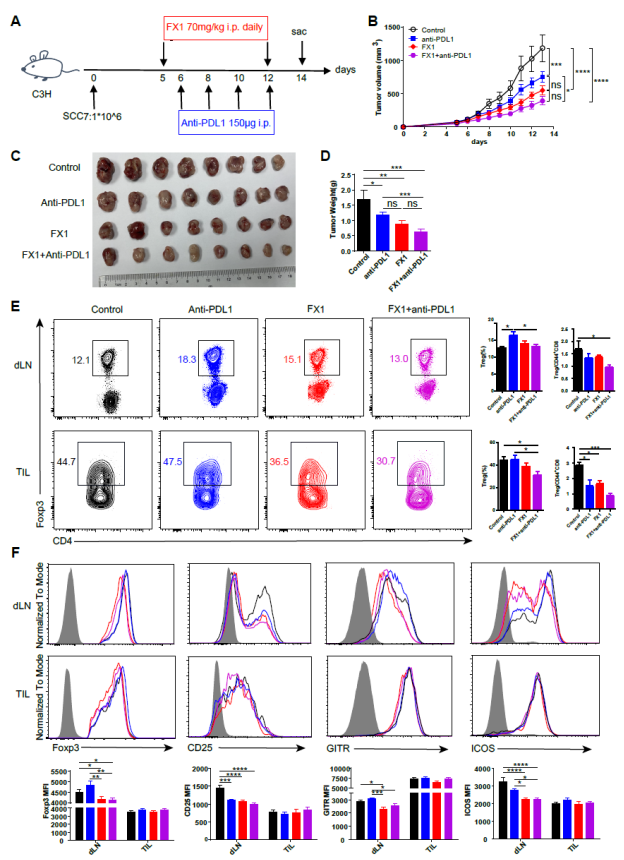
图4 FX1和ICB联合治疗可抑制小鼠HNSCC的肿瘤生长(原文中Figure 5)
综上所述,该研究揭示Bcl6在HNSCC进展中对维持Treg细胞谱系稳定性及免疫抑制功能具有关键作用。Treg细胞中Bcl6缺失可显著延缓4NQO诱导的HNSCC恶性转化进程。靶向抑制Bcl6不仅抑制小鼠HNSCC肿瘤生长,还能增强ICB治疗效果,提示Bcl6抑制剂有望成为HNSCC治疗中极具潜力的治疗靶点。
免费全文下载链接:
https://www.sciencedirect.com/science/article/pii/S2352304224003027
引用这篇文章:
Wen S, Su X, Guo J, et al. Bcl6 controls the stability and suppressive function of regulatory T cells in head and neck squamous cell carcinoma. Genes Dis. 2025;12(4):101505.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#Treg细胞# #头颈鳞癌#
11