减肥不只瘦体重!研究发现:脂肪细胞的 “衰老记忆” 能被擦掉,但免疫细胞还在 “记仇”
5小时前 梅斯内分泌新前沿 MedSci原创 发表于上海
研究揭示肥胖时脂肪组织免疫细胞入侵、细胞衰老,减重可逆转部分问题,但巨噬细胞存 “记忆”,为肥胖防治提供新方向。
健身房里,汗水浸透运动服的人们盯着电子秤上的数字暗自较劲;超市货架上,“低脂”“无糖”的标签成了抢手货;体检报告上,“BMI超标”的红色印章让无数人忧心忡忡……在这个被体重数字裹挟的时代,“减肥”早已不是个人选择,而是全球公共卫生的紧急命题。世界卫生组织的数据显示,全球已有超10亿人受肥胖困扰——这个数字比所有发达国家的人口总和还要多。但你或许不知道,在你为腰围增减一厘米而焦虑时,皮下那些看似不起眼的脂肪细胞,正在上演一场关乎健康的“变形记”。
脂肪组织,这个长期被贴上“赘肉”标签的身体成分,实则是维持代谢平衡的“能量调节器”。当我们摄入过多热量,脂肪细胞会像气球一样膨胀以储存能量;当能量短缺,它们又能分解脂肪释放燃料。可一旦“膨胀”失控,脂肪组织就会从“调节器”变成“麻烦制造者”:脂肪细胞撑得过大(肥大),免疫细胞趁机“入侵”,炎症因子四处游荡,血管和干细胞功能紊乱……最终引发糖尿病、心脏病等一串连锁反应。更棘手的是,即便成功减重,不少人还是会遭遇“反弹魔咒”,仿佛脂肪组织里藏着某种“记忆”。
为了揭开这场脂肪“变形记”的真相,来自伦敦帝国理工学院等机构的研究团队,带着70名志愿者的脂肪样本走进了实验室。他们中,有25人正经历着“从肥胖到减重”的蜕变(接受减肥手术后体重明显下降),24人则是体重正常的健康人。研究人员用单核RNA测序“透视”了17万余个脂肪细胞的基因活动,又通过空间转录组学给这些细胞“拍了全景照”,试图看清:肥胖时,脂肪组织里到底发生了哪些混乱?减重又能真正逆转多少问题?

脂肪组织的“肥胖乱局”:免疫细胞的“越界狂欢”
当研究人员用基因测序技术“放大”肥胖者的脂肪组织时,首先看到的是一场“免疫细胞大入侵”。在健康人的脂肪里,巨噬细胞(一种免疫细胞)的占比约14%,可到了肥胖者体内,这个数字飙升到31%,翻了一倍还多。这些“不速之客”中,不少是“脂质相关巨噬细胞”(LAM)——它们像贪婪的清道夫,围着脂肪细胞啃食多余的脂质,却也在这个过程中释放出大量炎症因子。
更有意思的是,这些巨噬细胞还分“善恶”。“善”的LAM忙着清理脂质,聚集在脂肪细胞死亡后形成的“冠样结构”周围;“恶”的LAM则单独行动,带着TLR2、TREM1等“炎症武器”,四处散播破坏信号,与胰岛素抵抗等代谢问题密切相关。与此同时,脂肪组织里的“原住民”——负责维持稳定的组织驻留巨噬细胞(TRM)却被挤到了角落,数量相对减少。
除了免疫细胞的“越界”,脂肪细胞自身也在“闹罢工”。肥胖者的成熟脂肪细胞数量明显减少,仿佛不堪重负纷纷“退场”;剩下的细胞里,不少呈现“应激”状态——JUN、NFKBIZ等应激基因高度活跃,像被过度拉伸的弹簧一样濒临崩溃;还有些细胞长满“纤维化”的“皱纹”,NOX4、LOX等基因的表达暴露了它们的衰老痕迹。这些“罢工”的脂肪细胞不仅无法正常储存或分解脂肪,连处理支链氨基酸(与胰岛素抵抗相关)的能力都大打折扣,整个代谢系统仿佛被按下了“混乱键”。
减重的“修复工程”:哪些细胞在认真“复工”?
当肥胖者通过手术或生活方式调整成功减重后,脂肪组织的“乱局”是否会彻底扭转?研究给出了一组喜忧参半的答案。
最显著的变化,是脂肪细胞的“重获新生”。减重后,“应激”脂肪细胞的比例从55%暴跌至14%,那些擅长合成脂质的“脂质生物合成细胞”则重新活跃起来。更关键的是,脂肪细胞的“代谢灵活性”回来了——它们不再是只会囤积脂肪的“懒人”,而是开启了“分解-合成”的循环模式:分解triglyceride(甘油三酯)释放能量,又重新合成新的脂质,这个看似“徒劳”的过程其实能清除有毒脂肪酸,就像给代谢系统“排毒”。支链氨基酸的处理能力也同步恢复,为改善胰岛素敏感性扫清了障碍。
另一大惊喜是“细胞衰老”的逆转。肥胖时,脂肪细胞、血管细胞和干细胞里充满了“衰老细胞”——它们停止分裂,却释放大量炎症因子“捣乱”。研究发现,减重像一把“衰老橡皮擦”,几乎清除了所有表达p21(衰老标志物)的细胞,让血管内皮细胞、脂肪前体细胞重新找回活力。原来,这些细胞的衰老与缺氧、机械压力有关,当脂肪细胞“瘦身”后,压力减轻,衰老信号自然减弱。
免疫细胞的“撤退”也很明显。减重后,巨噬细胞的占比从31%降至18%,淋巴细胞等“炎症推手”的数量也明显减少。但显微镜下的细节暴露了隐患:虽然炎症因子的释放减少了,但部分巨噬细胞的“代谢记忆”还在——它们的糖酵解、呼吸能力仍保持活跃,仿佛随时准备“卷土重来”。这或许能解释,为什么很多人减重后容易反弹:这些“潜伏”的免疫细胞可能是体重反弹的“内应”。
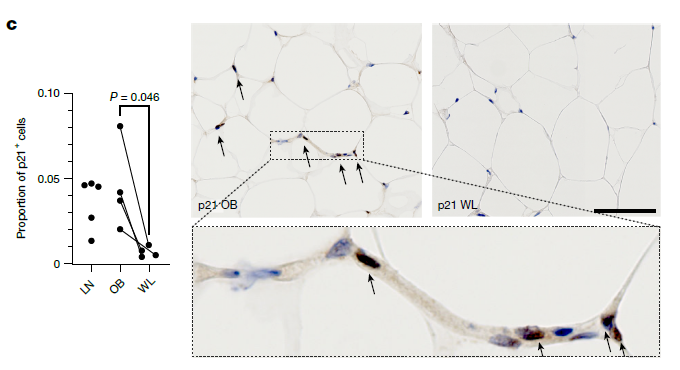
减重清除脂肪组织中的衰老细胞
脂肪“记忆”与健康密码:研究背后的临床启示
这场对脂肪组织的“显微探秘”,不仅解答了“肥胖为何致病”“减重为何有效”的科学谜题,更给肥胖防治提供了新的突破口。
首先,“逆转衰老”可能是减重改善代谢的核心机制。研究发现,脂肪组织中的衰老细胞会引发“退化循环”:衰老导致炎症,炎症加速更多细胞衰老,最终陷入代谢紊乱。而减重能打断这个循环,这意味着未来或许能开发“抗衰药物”,针对性清除脂肪中的衰老细胞,帮助代谢恢复。
其次,巨噬细胞的“持续激活”提示我们:减重不是终点,而是“持久战”。这些带着“记忆”的免疫细胞可能是体重反弹的关键,因此在减重后,或许需要针对性调节免疫状态,比如通过饮食或药物抑制其过度激活,才能巩固成果。
最后,脂肪细胞的“代谢灵活性”为减肥方法提供了新思路。研究发现,减重后脂肪细胞的“脂质循环”(分解与合成的平衡)很活跃,这需要消耗能量——这意味着,与其一味“节食饿肚子”,不如通过合理运动和饮食,让脂肪细胞保持“动态平衡”,既能高效供能,又不囤积毒素。
当然,这项研究也有其局限:它主要关注腹部皮下脂肪,而内脏脂肪的变化还不明确;研究对象未包含糖尿病患者,难以反映更复杂的代谢状态。但这并不影响其价值——它像一台“细胞显微镜”,让我们看清了脂肪组织的“健康密码”:肥胖不是脂肪的“原罪”,而是其“变形”失控的结果;减重的意义,不仅是数字的减少,更是让脂肪细胞找回“平衡之道”。
或许未来某天,当我们再站到体重秤上时,关注的不再只是数字的增减,而是皮下那些细胞是否在健康地“呼吸”与“工作”。毕竟,真正的健康,从来都藏在微观世界的平衡里。
参考文献:
Miranda, A.M.A., McAllan, L., Mazzei, G. et al. Selective remodelling of the adipose niche in obesity and weight loss. Nature (2025). https://doi.org/10.1038/s41586-025-09233-2
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#肥胖# #脂肪组织#
4 举报