NEJM:贝伐珠单抗联合厄洛替尼治疗 HLRCC 相关乳头状肾癌,一项II期临床试验成果解析
2025-06-19 MedSci原创 MedSci原创 发表于上海
HLRCC患者中位无进展生存期达21.1个月,整体生存期中位数达44.6个月,治疗效果耐久且临床意义突出。
乳头状肾细胞癌(papillary renal-cell carcinoma, PRCC)是肾癌的第二大病理亚型,既包括散发型也包括遗传性亚型。肾细胞癌综合征(HLRCC)是一种罕见的常染色体显性遗传病,因细胞中丝氨酸水合酶(fumarate hydratase, FH)基因病理性变异导致高致癌风险,患者肾癌常呈侵袭性和进展迅速,缺乏有效系统治疗手段,预后极差。HLRCC相关肾癌的分子病理基础包括FH缺失引起的代谢重编程(沃伯格效应)、组织内琥珀酸积累稳定HIF,进而激活VEGFA及EGFR信号通路,对这些通路的靶向抑制或可实现治疗突破。
尽管抗VEGF单抗(如贝伐珠单抗)及EGFR抑制剂(如厄洛替尼)在其他肿瘤中已获得疗效,针对HLRCC的联合方案开展的临床研究不足,近期发表于新英格兰医学杂志的一项开放标签、II期临床研究,系统评估了贝伐珠单抗与厄洛替尼联合用药在晚期遗传性纤维瘤病和HLRCC相关及散发型乳头状肾细胞癌患者中的疗效和安全性。研究共纳入83例患者(43例HLRCC相关,40例散发型),为此类罕见疾病提供了宝贵的临床循证依据。

本研究为美国国立癌症研究所开展的开放标签、单臂II期临床试验。主要纳入符合RECIST 1.1标准的晚期HLRCC相关或散发型乳头状肾癌患者。给予贝伐珠单抗(10 mg/kg静脉输注,每两周一次)联合每日服用厄洛替尼(150 mg口服),每周期28天。主要终点为总体缓解率(ORR),次要终点包括无进展生存期(PFS)、总生存期(OS)及治疗安全性。根据IMDC风险分层评估患者预后并进行亚组分析。
结果详述
- 患者基线特征
- HLRCC相关群体(n=43)中,中位年龄43岁,男性占70%,所有患者均呈转移期(M1期),优良风险(26%),中度风险(56%),差风险(19%)。21%既往接受系统治疗,其中多数曾用VEGFR抑制剂。
- 散发型PRCC患者(n=40)中,中位年龄55.5岁,男性占65%,优良风险仅8%,多数为中度风险(72%),45%既往经治疗。
- 疗效数据汇总:
| 指标 | HLRCC-associated PRCC (n=43) | Sporadic PRCC (n=40) |
|---|---|---|
| 总体缓解率(ORR) | 72%(95% CI 57-83) | 35%(95% CI 22-51) |
| 完全缓解率 (CR) | 5% | 0% |
| 部分缓解率 (PR) | 67% | 35% |
| 中位无进展生存期(PFS,月) | 21.1(95% CI 15.6-26.6) | 8.9(95% CI 5.5-18.3) |
| 中位总生存期(OS,月) | 44.6(95% CI 32.7-未达到) | 18.2(95% CI 12.6-29.3) |
| 中位反应维持时间(DoR,月) | 19.3(95% CI 12.9-35.9) | 18.4(95% CI 13.8-49.7) |
| 2年以上持续用药比例 | 35% | 15% |
患者绝大多数在治疗早期即产生反应(中位反应时间约1.8个月)。未缓解患者均表现为疾病稳定,其中部分患者稳定时间超过6个月。HLRCC患者不同IMDC风险组均可见反应。既往接受系统治疗者,整体生存率较未治疗组有所降低。
- 安全性分析:所有患者均报告至少一种治疗相关不良事件(AEs)。最常见轻度或中度AEs为:
- 皮肤红疹(93%),腹泻(89%),蛋白尿(78%)。
3级及以上不良事件中,最突出为: - 高血压(34%),蛋白尿(17%),腹泻(5%),皮疹(5%)。
药物剂量调整主要针对厄洛替尼,24例患者接受减量,仅1例因皮肤毒性停止用药。贝伐珠单抗剂量减量不予许可,亦有极少数因冠状动脉综合征等严重不良反应停药。总体不良事件符合已知药物安全谱,且能通过对症支持治疗管理。
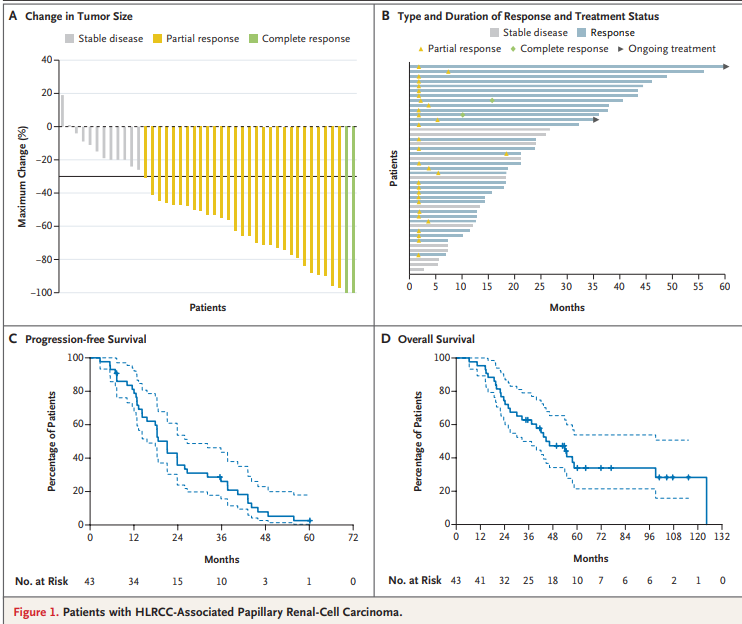
HLRCC相关乳头状肾癌患者治疗响应及生存分析
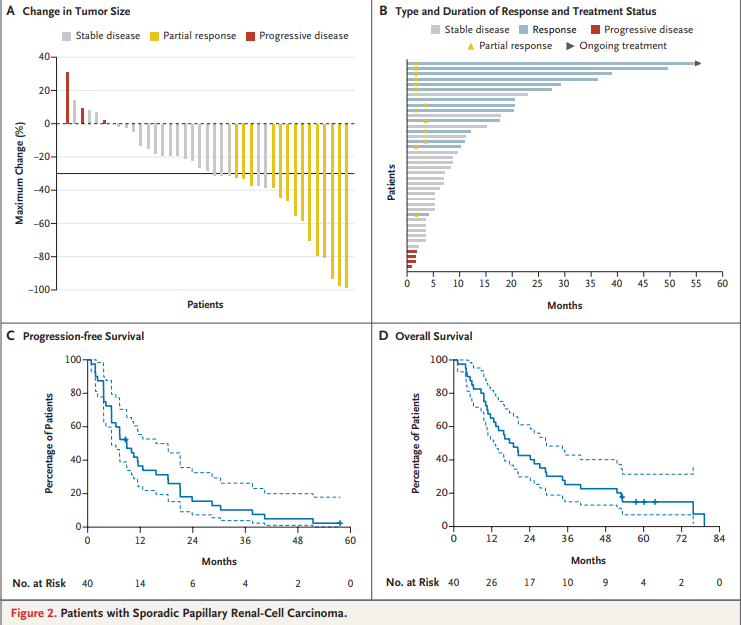
散发型乳头状肾癌患者治疗响应及生存分析
研究价值与意义
HLRCC相关乳头状肾癌是一种恶性程度高、缺乏有效治疗方案的罕见肾癌亚型。本研究首次通过II期临床试验表明针对FH缺失引发的代谢和信号转导异常设计的双靶点联合治疗,能显著提升患者的缓解率和生存期。贝伐珠单抗阻断VEGFA介导的肿瘤血管生成,厄洛替尼抑制EGFR下游信号传导,协同作用正中肿瘤增殖和代谢的关键枢纽,打破了肿瘤细胞对恶劣代谢环境的适应。
尽管散发型乳头状肾癌的反应率不及HLRCC相关患者,联合治疗所获得的持续反应及生存期延长仍显示出潜在的临床应用价值。此外,该研究证实了FH缺失肾癌的独特生物学特征与靶向治疗培育的精准医疗理念间的契合点,推动了肾癌亚型精准分层及治疗策略制定。
不良事件谱与此前贝伐珠单抗和厄洛替尼单药或联合治疗其他实体瘤时观察到的相符,治疗可耐受且管理措施明确,为临床推广提供了安全基础。
未来研究有望深入挖掘联合治疗产生耐药的分子机制,为机制驱动的二线治疗以及联合免疫治疗方案铺路。同时,多中心大规模随机临床试验的开展,将进一步验证疗效,为HLRCC患者确立标准治疗方案奠定基础。
梅斯小编点评
贝伐珠单抗联合厄洛替尼针对HLRCC相关乳头状肾癌的突破性疗效,标志着肾癌治疗迈入靶向代谢和信号双路径的新纪元。这项研究不仅展现了精准医学的临床转化能力,更体现了对罕见遗传性肿瘤深入分子机理的解读带来的实际临床价值。未来结合免疫调节剂、开发耐药逆转策略,以及对FH通路进一步精细刻画,将成为提升患者长期获益和生存质量的关键方向。对肾癌患者而言,这无疑是充满希望的进展。
原始出处
Srinivasan R, Gurram S, Singer EA, et al. Bevacizumab and Erlotinib in Hereditary and Sporadic Papillary Kidney Cancer. N Engl J Med. 2025;392(23):2346-2356. DOI: 10.1056/NEJMoa2200900.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#乳头状肾细胞癌# # HLRCC 相关乳头状肾癌#
12 举报