NEJM:贝达喹啉(Bedaquiline)治疗麻风病的最新临床研究进展
昨天 MedSci原创 MedSci原创 发表于加利福尼亚
贝达喹啉(Bedaquiline,BDQ)是一种新型抗结核药物,首次成功应用于麻风病患者的临床研究。通过开放标签试验,30例多菌型麻风患者接受BDQ单药治疗,结果显示治疗56天后,绝大多数患者皮肤组织
Highlight
- 贝达喹啉(Bedaquiline,BDQ)为抗结核一线新药,首次被证实在人体麻风病患者中具有显著杀菌活性。
- 单独短期BDQ治疗即能大幅减少皮肤中的麻风分枝杆菌数量及活性,缩短治疗时间潜力巨大。
- BDQ4LEP临床试验显示,BDQ单药56天治疗后,24/25患者皮损菌株培养转为阴性,无观察到复发病例,提示其安全有效。
研究概述
2025年6月5日,《新英格兰医学杂志》(N Engl J Med)刊登了题为“Bedaquiline Activity against Leprosy”的研究信件,报道了贝达喹啉(BDQ)对麻风分枝杆菌(Mycobacterium leprae)的杀菌活性。麻风病是由不可体外培养的麻风杆菌感染引起的慢性传染病,全球每年约新增20万例病例。传统多药联合治疗(MDT)疗程长达12个月,且面临耐药性和副作用挑战。本研究旨在评估BDQ作为一种潜在的新型抗麻风药物,在人体患者中的疗效和安全性,为优化麻风病治疗方案提供依据。
背景介绍
麻风病因麻风分枝杆菌感染所致,该病原体无法培养,给临床治疗和研究带来巨大难题。虽然目前使用的多药联合治疗(MDT)在控制病情方面较为有效,但疗程冗长且继续存在耐药和毒副作用问题。贝达喹啉作为一种新型日内酰胺类药物,靶向阻断细菌ATP合酶,已被成功应用于耐多药结核病治疗中,具有显著的抗菌效果和缩短疗程的能力。既往动物模型研究显示,低剂量BDQ对麻风分枝杆菌同样有效,提示BDQ可能成为麻风病治疗的新选择。
研究方法
本研究为开放标签临床试验(BDQ4LEP,注册号PACTR202408643515316),在马里巴马科单中心进行,纳入30例未经治疗的多菌型(multibacillary)麻风病患者。该试验经相关伦理委员会批准,所有参与者均签署知情同意书。
- 用药方案:
- 200 mg BDQ每日一次,连续2周(14天)
- 随后100 mg BDQ每周3次,持续6周
- 之后患者接受标准12个月多药联合治疗(MDT),且随访12个月监测复发情况。
- 皮肤切片活检分别在治疗第0天(D0),第56天(D56,即BDQ单药治疗结束后)和MDT结束时采集。
- 评估指标包括细菌学指标(显微镜下菌指数及形态学指数)、分子生物标志物(细菌DNA RLEP序列及mRNA水平)、以及小鼠足垫培养确认活菌数量。
研究结果
-
菌落学和显微镜指标变化
17名完成全程BDQ及MDT治疗患者的切片显示,菌指数(Bacteriological Index,BI)和形态学指数(Morphological Index,MI)在治疗过程中明显下降(见图1A,1C)。
-
DNA和mRNA分子生物标志物
通过qPCR检测RLEP DNA的拷贝数,整体呈现出缓慢下降趋势,但治疗结束时仍低水平检测到细菌DNA(图1B)。mRNA水平(_esxA_和_hsp18_基因表达)在D56时显著减少,MDT结束后已无可检测到的mRNA,表明细菌活性显著降低甚至消失(图1D)。
-
小鼠足垫培养检测
30个D0病灶切片全部培养阳性,表明活菌存在。治疗56天后,25个切片中有24个(96%)培养阴性,仅1例仍示存活细菌。MDT治疗完成的17名患者皮肤样本均为培养阴性。随访12个月无复发报告(图1E)。
表1:治疗关键指标的量化变化(17名完成治疗患者)
| 时间点 | 菌指数(BI) | 形态学指数(MI) | RLEP DNA拷贝数(平均) | mRNA表达水平(%基线) |
|---|---|---|---|---|
| 第0天 (D0) | 4.5 | 30% | 1.0 | 100% |
| 第56天 (D56) | 1.8 | 10% | 约0.6 | 约20% |
| 多药治疗结束 | 0.1 | 0% | 约0.1 | 0% |
图1:BDQ治疗期间的生物标志物变化
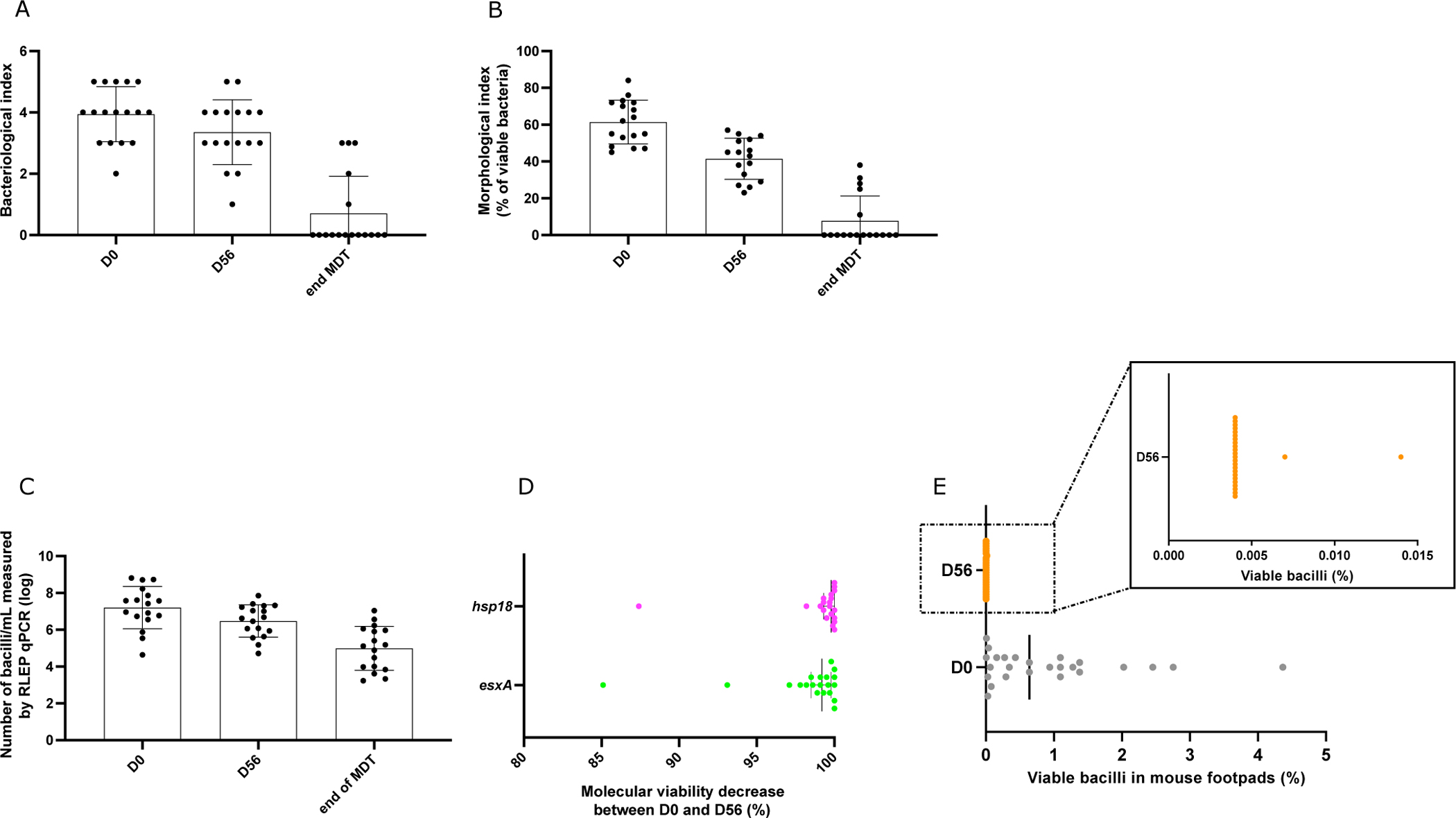
- A. 菌指数随治疗时间的下降趋势
- B. RLEP DNA拷贝数的变化
- C. 形态学指数的变化
- D. mRNA表达水平的降低
- E. 小鼠培养的活菌百分比显著下降
研究价值与意义
BDQ4LEP研究首次在人类麻风患者中验证了贝达喹啉的显著杀菌活性,临床短期单药治疗即能有效抑制麻风分枝杆菌生长,且安全耐受良好。该研究为BDQ作为缩短麻风病治疗时间的新策略提供了强有力的证据支持,同时为抗麻风病药物研发开辟了新方向。未来,BDQ有望联合现有疗法,优化麻风病治疗,有效降低抗药性发生及治疗副作用负担。
梅斯编辑点评
麻风病治疗长期以来受限于疗程长、耐药增加及副作用风险,“安全、有效且疗程短”的抗麻风药物极为稀缺。贝达喹啉作为革新抗结核药物,展现出跨疾病治疗潜力,本研究采用严谨的分子和细菌学监测方法,全面评估了BDQ杀菌效果,结果鼓舞人心。特别是小鼠培养系统验证活菌清除实证,有助于临床决策。该研究为临床及公共卫生领域麻风病治疗模式变革提供新契机,值得进一步大规模多中心临床试验验证。
参考文献
-
World Health Organization. Global leprosy update, 2017: reducing the disease burden due to leprosy. Weekly Epidemiol Rec. 2018;93(36):445-456.
-
Andries K, Verhasselt P, Guillemont J, et al. A diarylquinoline drug active on the ATP synthase of Mycobacterium tuberculosis. Science. 2005;307(5707):223-227. doi:10.1126/science.1106753.
-
Conradie F, Diacon AH, Ngubane N, et al. Treatment of Highly Drug-Resistant Pulmonary Tuberculosis. N Engl J Med. 2020;382(10):893-902. doi:10.1056/NEJMoa1901814.
-
Gelber R, Andries K, Paredes RM, Andaya CE, Burgos J. The diarylquinoline R207910 is bactericidal against Mycobacterium leprae in mice at low dose and administered intermittently. Antimicrob Agents Chemother. 2009;53(9):3989-3991. doi:10.1128/AAC.00722-09.
-
Davis GL, Ray NA, Lahiri R, et al. Molecular assays for determining Mycobacterium leprae viability in tissues of experimentally infected mice. PLoS Negl Trop Dis. 2013;7(8):e2404. doi:10.1371/journal.pntd.0002404.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#分子标志物# #麻风病# #多药联合治疗# #贝达喹啉#
11